��Ŀ����
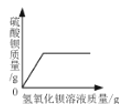
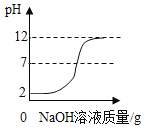
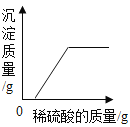
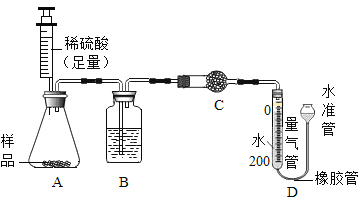
����Ŀ��ʵ��Ա����ʦҪ����80g��������Ϊ10%��NaOH��Һ��ͬѧ��ʹ�ã���ͼ��ʾ������ʵ��������̡�
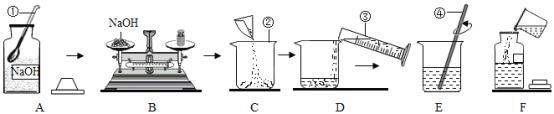
�ش��������⣺
��1��д�����������Ƣ�_____��_____
��2��B��������һ��������_____��Ӧ��NaOH��������_____g��������������ָ��ƫ��Ӧ���еIJ�����_____��
��3�������۵Ĺ��Ӧ��_____��ѡ�50mL����100mL��������ȡˮʱ���������⣬����Ҫ��һ��������_____��
��4��E�����Тܵ�������_____��
��5�����д���������ܵ������ʵ���������ƫС����_____������ţ���
��B������������NaOH�ŵߵ��ˣ�1g���������룩
��C������ʹ�õ��ձ��ڱ���ˮ
������Ͳ��ˮʱ���Ӱ�Һ����ʹ�����
��F��������Һ����
���𰸡�ҩ�� �ձ� ��������û�з��ڲ��������г��� 8.0 ��������ȡ������ҩƷ����ƽƽ�� 100mL ��ͷ�ι� ���裬�ӿ��ܽ����� �٢ڢ�
��������
��1�����������Ƣ���ҩ�ף������ձ���
��2���������ƾ��и�ʴ�ԣ����ܷ���ֽ�ϳ�����Ҫ���ڲ��������г�������B��������һ����������������û�з��ڲ��������г���������80g��������Ϊ10%��NaOH��Һ����Ӧ��NaOH��������![]() ��������������ָ��ƫ��˵���������Ƶ���̫���ˣ���Ӧ���еIJ����Ǵ�������ȡ������ҩƷ����ƽƽ�⡣
��������������ָ��ƫ��˵���������Ƶ���̫���ˣ���Ӧ���еIJ����Ǵ�������ȡ������ҩƷ����ƽƽ�⡣
��3������80g��������Ϊ10%��NaOH��Һ��ˮ������Ϊ![]() ��ˮ�����Ϊ
��ˮ�����Ϊ![]() ����Ͳѡ�����ȡ��Һ������ӽ������̣��������۵Ĺ��Ӧ��100mL����ȡˮʱ���㵹���ӽ��̶��ߴ���Ȼ���ý�ͷ�ιܵμ����̶��ߣ��ʳ��������⣬����Ҫ��һ�������ǽ�ͷ�ιܡ�
����Ͳѡ�����ȡ��Һ������ӽ������̣��������۵Ĺ��Ӧ��100mL����ȡˮʱ���㵹���ӽ��̶��ߴ���Ȼ���ý�ͷ�ιܵμ����̶��ߣ��ʳ��������⣬����Ҫ��һ�������ǽ�ͷ�ιܡ�
��4��E�����Т��Dz��������������ǽ��裬�ӿ��ܽ����ʡ�
��5����B������������NaOH�ŵߵ��ˣ�1g���������룩����ʹ�������Ƶ��������٣��������ʵ���������ƫС������ȷ��
��C������ʹ�õ��ձ��ڱ���ˮ��ˮ�����ƫ�������ʵ���������ƫС������ȷ��
������Ͳ��ˮʱ���Ӱ�Һ����ʹ�����������ƫС��ʵ����ȡˮ�����ƫ�������ʵ���������ƫС������ȷ��
��F��������Һ���䣬���ʵ������������䣬�ʲ���ȷ��
��ѡ�٢ڢۡ�

 �����ҵ���������ͯ������ϵ�д�
�����ҵ���������ͯ������ϵ�д�����Ŀ����ѧ��ȤС���ijƷ�������е�Ħ�����ɷּ��京����������̽����
��������ϣ�
��1��������Ħ������̼��ơ�����������ɣ������������ɷ���������ʱ�����������
��2������̼��������Һ�����ն�����̼��
��3����ʯ�ҵ���Ҫ�ɷ�Ϊ�����ƺ��������ơ�
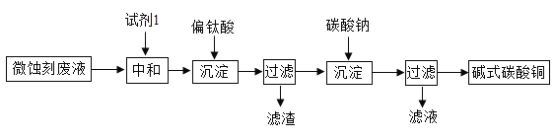
�����ʵ�飩С��ͬѧ�������ͼ��ʾװ�ã�ͼ�мг�������ȥ���ⶨ������Ʒ��̼��Ƶĺ�����
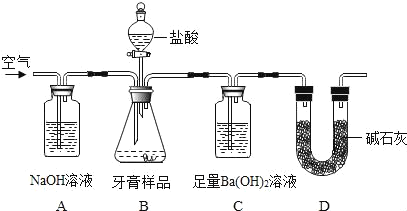
����ͼʾ�ش��������⣺
��1��Bװ��ʹ�÷�Һ©�����ŵ���_____��
��2��A������������Һ��������_____��
��3��C�й۲쵽�г�����������Ӧ�Ļ�ѧ����ʽΪ_____��
��4��ʵ����������������ͨ���������������_____��
����������ۣ���C�в�������ͨ��_____��ϴ�ӡ����������ͨ���������������Ʒ��̼��Ƶĺ�����
����˼�����ۣ�
��˼ʵ����̣�С��ͬѧ���Ӧ��ȡ��Ҫ��ʩ����߲ⶨȷ�ȡ�����������и����ʩ�У�������߲ⶨȷ�ȵ���_____������ĸ��ţ���
a �ڼ�������֮ǰ���ž�װ���ڵ�CO2����
b �����μ�������ٶ�
c ��A��B֮������ʢ��Ũ�����ϴ��װ��
d ��B��C֮������ʢ�б���̼��������Һ��ϴ��װ��
����չ���죩С��ͬѧΪȷ��A�����ʳɷ֣������������ʾʵ�飺
ʵ����� | ʵ������ | ʵ����� |
��1����ȡ������Һ���Թ��У���������____ | ������ɫ���� | ������Ҫ�ɷ�ΪNa2CO3��NaOH |
��2�������ˣ�ȡ������Һ���� | _____ |