题目内容
解决问题常面临着方法的选择,面对不同的结果我们应继续探索。为得知15.8 g高锰酸钾完全分解能产生多少克氧气,小柯与小妍分别采取了以下方法:
| 小柯:实验测定法 | 小妍:计算法 |
| 小柯在老师的指导下,将15.8g高锰酸钾充分加热,得到氧气1300mL。 | 解:高锰酸钾中氧元素的质量分数 =×100%21世纪教育网 = 氧气的质量为:15.8g×40.5%=6.4g
|
请回答:
(1)在本实验条件下,氧气的密度为1.4×10-3g/mL,则由小柯的测量结果可算出
15.8 g高锰酸钾分解后所产生的氧气质量为——g(结果保留一位小数)。
(2)大家经过讨论,认为小妍的计算方法明显错误,本题不能采用该方法计算氧气质
量的一项理由是( )。
A.高锰酸钾中含氧元素
B.锰酸钾和二氧化锰中含氧元素
C.氧气中含氧元素
(3)请计算15.8 g高锰酸钾完全分解所产生的氧气质量为____________________g。
(4)![]() 若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,
若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,
请提出一种合理的猜测:_______________________________。
答案:(1)1.8 (2)B (3) 1.6 (4)可能是生成K2MnO4分解放出了氧气(或生成含氧化合物有一部分分解释放了氧气)。

 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案| 小柯:实验测定法 | 小妍:计算法 | ||||
| 小柯在老师的指导下,将15.8g高锰酸钾充分加热,得到氧气1300mL. | 解:高锰酸钾中氧元素的质量分数=
=
=40.5% 氧气的质量为15.8g×40.5%=6.4g 答:15.8g高锰酸钾完全分解产生氧气6.4g. |
(1)在本实验条件下,氧气的密度为1.4×l0-3g/mL,则由小柯的测量结果可算出15.8 g高锰酸钾分解后所产生的氧气质量为
(2)大家经过讨论,认为小妍的计算方法明显错误,本题不能采用该方法计算氧气质量的一项理由是
A.高锰酸钾中含氧元素B.锰酸钾和二氧化锰中含氧元素C.氧气中含氧元素
(3)请计算15.8 g高锰酸钾完全分解所产生的氧气质量.(写出解题过程)
(4)若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,请提出一种合理的猜测:
解决问题常面临着方法的选择,面对不同的结果我们应继续探索。为得知15.8 g高锰酸钾完全分解能产生多少克氧气,小柯与小妍分别采取了以下方法:
| 小柯:实验测定法 | 小妍:计算法 |
| 小柯在老师的指导下,将15.8g高锰酸钾充分加热,得到氧气1300mL。 | 解:高锰酸钾中氧元素的质量分数
= 氧气的质量为:15.8g×40.5%=6.4g 答:15.8g高锰酸钾完全分解产生氧气6.4g。 |
请回答:
(1)在本实验条件下,氧气的密度为1.4×10-3g/mL,则由小柯的测量结果可算出
15.8 g高锰酸钾分解后所产生的氧气质量为——g(结果保留一位小数)。
(2)大家经过讨论,认为小妍的计算方法明显错误,本题不能采用该方法计算氧气质
量的一项理由是( )。
A.高锰酸钾中含氧元素
B.锰酸钾和二氧化锰中含氧元素
C.氧气中含氧元素
(3)请计算15.8 g高锰酸钾完全分解所产生的氧气质量为____________________g。
(4)若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,
请提出一种合理的猜测:_______________________________。
解决问题常面临着方法的选择,面对不同的结果我们应继续探索。为得知15.8 g高锰酸钾完全分解能产生多少克氧气,小柯与小妍分别采取了以下方法:
小柯:实验测定法 | 小妍:计算法 |
小柯在老师的指导下,将15.8g高锰酸钾充分加热,得到氧气1300mL。 | 解:高锰酸钾中氧元素的质量分数
= 氧气的质量为:15.8g×40.5%=6.4g 答:15.8g高锰酸钾完全分解产生氧气6.4g。 |
请回答:
(1)在本实验条件下,氧气的密度为1.4×10-3g/mL,则由小柯的测量结果可算出
15.8 g高锰酸钾分解后所产生的氧气质量为——g(结果保留一位小数)。
(2)大家经过讨论,认为小妍的计算方法明显错误,本题不能采用该方法计算氧气质量的一项理由是( )。
A.高锰酸钾中含氧元素
B.锰酸钾和二氧化锰中含氧元素
C.氧气中含氧元素
(3)请计算15.8 g高锰酸钾完全分解所产生的氧气质量为____________________g。
(4)若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,
请提出一种合理的猜测:_______________________________。
| 小柯:实验测定法 | 小妍:计算法 |
| 小柯在老师的指导下,将15.8g高锰酸钾充分加热,得到氧气1300ml. | 解:高锰酸钾中氧元素的质量分数= ×100% ×100%= 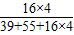 ×100% ×100%=40.5% 氧气的质量为15.8g×40.5%=6.4g 答:15.8g高锰酸钾完全分解产生氧气6.4g. |
(1)在本实验条件下,氧气的密度为1.4×l0-3g/mL,则由小柯的测量结果可算出15.8 g高锰酸钾分解后所产生的氧气质量为______g(结果保留一位小数).
(2)大家经过讨论,认为小妍的计算方法明显错误,本题不能采用该方法计算氧气质量的一项理由是______.
A.高锰酸钾中含氧元素B.锰酸钾和二氧化锰中含氧元素C.氧气中含氧元素
(3)请计算15.8 g高锰酸钾完全分解所产生的氧气质量.(写出解题过程)
(4)若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,请提出一种合理的猜测:______.

 ×100%
×100%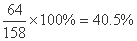
 ×100%
×100%