��Ŀ����
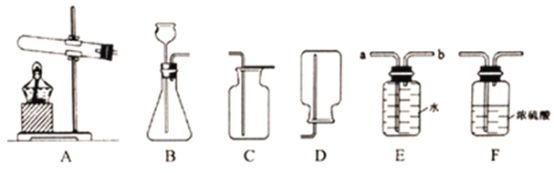
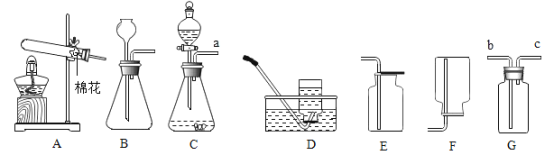
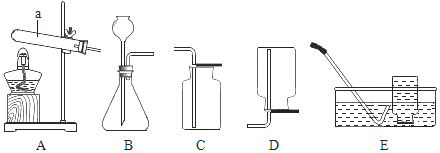
����Ŀ������ͼ��ʾװ�ã��ڳ����·ֱ����̽����ȼ��ȼ�������������������ʵ�ʵ�顣
��֪�������Ż��Ϊ40��
���� װ�� | ��ʵ��1�� ̽����ȼ��ȼ������ | ��ʵ��2�� ̽�������������� |
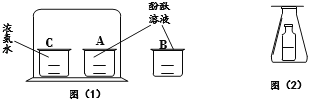
| I. A��ʢ��H2O2��Һ��B��ʢ��MnO2��C��ʢ��80�����ˮ��һС����� | I. A��ʢ�е��з�̪�� NaOH��Һ��B�г���CO2��C��ʢ��ϡ���� |
II. ��Һ©����������A����Һ�μӵ�B�У��رշ�Һ©����������K | II. ��Һ©����������A����Һ�μӵ�B�У��رշ�Һ©����������ַ�Ӧ��K |
(1)H2O2��Һ��MnO2�Ӵ�ʱ��������Ӧ�Ļ�ѧ����ʽΪ______��
(2)ʵ��1�У���K��۲쵽C�а���ȼ�ա���ʵ��֤����ȼ��ȼ�յ�����֮һ��_______��
(3)ʵ��2�У��������۲쵽����������ʵ������C�в���Һ���ص�������B�У�B�����������ɣ�B����Һ�ɺ�ɫ��Ϊ��ɫ�����Ͳ��������������Ҫԭ��_______(�û�ѧ����ʽ��ʾ)��
���𰸡� 2H2O2![]() 2H2O + O2���������Ӵ�CO2 + 2NaOH = Na2CO3 + H2O��Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2��(�����𰸺�������)
2H2O + O2���������Ӵ�CO2 + 2NaOH = Na2CO3 + H2O��Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2��(�����𰸺�������)
��������
(1)H2O2��Һ��MnO2�Ӵ�ʱ�����������ڶ�������������������������ˮ����������Ӧ�Ļ�ѧ����ʽΪ��2H2O2![]() 2H2O + O2����(2)ʵ��1�У���K��۲쵽C�а���ȼ�գ���ʵ��֤����ȼ��ȼ�յ�����֮һ�ǣ���ȼ��ȼ����Ҫ������(3)ʵ��2�У�������̼���������Ʒ�Ӧ����̼���ƺ�ˮ��̼���ƺ����ᷴӦ���������ƺ�ˮ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ��CO2+2NaOH=Na2CO3+H2O��Na2CO3+H2SO4=Na2SO4+H2O+CO2��(�𰸺�������)��
2H2O + O2����(2)ʵ��1�У���K��۲쵽C�а���ȼ�գ���ʵ��֤����ȼ��ȼ�յ�����֮һ�ǣ���ȼ��ȼ����Ҫ������(3)ʵ��2�У�������̼���������Ʒ�Ӧ����̼���ƺ�ˮ��̼���ƺ����ᷴӦ���������ƺ�ˮ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ��CO2+2NaOH=Na2CO3+H2O��Na2CO3+H2SO4=Na2SO4+H2O+CO2��(�𰸺�������)��

����Ŀ��NH4Cl��Na2SO4���ܽ�ȱ����ܽ��������ͼ������˵���������( )

�¶�/�� | 10 | 20 | 30 | 40 | 50 | 60 | |
�ܽ��S/g | NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
A. ��ΪNH4Cl
B. t3Ӧ����40����50��
C. 55��ʱ���ֱ���������Һ������������ˮ���õ����������ף���
D. �������ļס��ұ�����Һ��t3���µ�t1�������ľ����������