题目内容
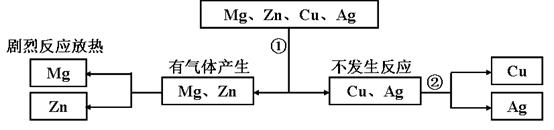
向FeCl2和CuCl2的混合溶液中加入一定量的镁粉,当反应停止后过滤,向滤出的固体中滴加盐酸,没有气体产生。则滤液中的溶质是
| A.只有MgCl2 | B.只有MgCl2和FeCl2,一定没有CuCl2 |
| C.只有FeCl2 | D.一定有MgCl2和FeCl2,可能有CuCl2 |
D
试题分析:根据金属活动性顺序分析,向FeCl2和CuCl2的混合溶液中加入一定量的镁粉, Mg与FeCl2和CuCl2都能发生置换反应,生成相应的金属Fe、Cu和氯化镁;同时Mg与FeCl2反应生成的Fe也能与CuCl2发生置换反应,生成Cu和FeCl2,由此可知,Mg会先置换出最不活泼的Cu,然后再置换出比铜活泼的铁。
再结合题意分析,当反应停止后过滤,向滤出的固体中滴加盐酸,没有气体产生,说明置换出来的金属中只有铜,没有铁和镁,也就是说FeCl2没有发生置换反应,即滤液中一定含有FeCl2;由于镁粉的量不确定,故不能确定CuCl2是否完全反应,即滤液中不一定含不含有CuCl2。故选D
点评:在金属活动性顺序中只要排在前面的金属就能把排在后面的金属从其盐溶液中置换出来;用同种金属置换不同的盐溶液,盐中金属排在金属活动性顺序中较后的金属首先被置换出来,用不同的金属置换同种盐溶液,盐中金属先被排在金属活动性顺序中较前的金属置换出来。

练习册系列答案
相关题目