题目内容
某兴趣小组的同学为探究金属的活动性、以及铜锈蚀的条件进行了以下系列
实验,仔细分析后回答下列问题:
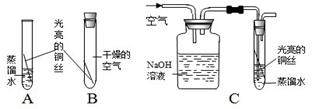
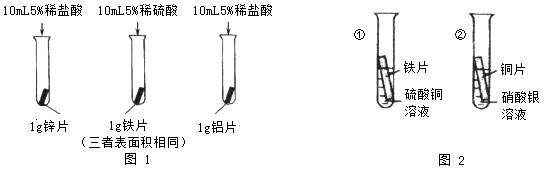
(1)实验一:小明按下图1所示以“金属表面产生气泡的快慢”为标准来判断锌、铝、铁
的活动性强弱,有同学认为不够合理,理由是________________________________。铝与
稀盐酸刚接触时反应缓慢,一段时间后剧烈,产生气泡速率随着加快,其原因可能是
_________________________________________。
(2)实验二:为探究铁、铜、银三种金属活动性的顺序,小红提出按上图2进行两步实验,
即可证明三种金属活动性顺序。你认为其方案可行吗?_______(填“可行”或“不可行”) 。
a. 试管①中现象是________________________________________________。
b. 试管②中发生反应的化学方程式为________________________________________。
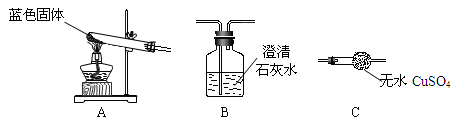
(3)实验三:小芳、小亮两位同学发现铜质眼镜架上出现了一些绿色的锈渍。经查阅资料得知,铜锈的化学成分是碱式碳酸铜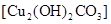 。他们依照钢铁生锈的探究方法设计如下实验(下图3所示)。请回答:
。他们依照钢铁生锈的探究方法设计如下实验(下图3所示)。请回答: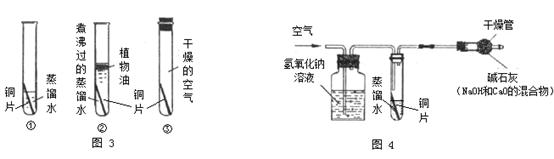
a. 推测一段时间后会出现铜锈的是________试管内的铜片。(填“①”、“②”或“③”)
b. 小芳同学认为要弄清导致铜锈蚀的因素,还应该补充实验,如上图4所示的实验,其目
的是________________________________________________________________。
⑴选取酸的种类不同 铝表面的氧化膜没有完全去掉,先与稀盐酸反应
⑵可行 a. 铁片上覆盖一层红色的固体物质,溶液由蓝色逐渐变为浅绿色
b. 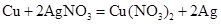
⑶a. ①
b.证实二氧化碳也是导致铜生锈的因素之一
解析试题分析:(1)判断金属活动性的强弱要采用控制变量法,即金属不同,其它的要完全相同,由于铝在空气中易被氧化,故金属铝要先打磨把表面的氧化物除去;
(2)铁能把硫酸铜中的铜置换出来,说明铁的活动性大于铜的活动性,铜能把硝酸银中的银置换出来,说明铜的活动性比银强,故能得出金属活动性顺序,该方案可行;
(3)根据碱式碳酸铜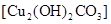 的化学式,依据质量守恒定律化学反应前后元素的种类不变可知,铜生锈的条件有:水、氧气、二氧化碳,只有①满足条件;图4所示的实验中用氢氧化钠溶液吸收空气中的二氧化碳,结果铜没有生锈,证实二氧化碳也是导致铜生锈的因素之一。
的化学式,依据质量守恒定律化学反应前后元素的种类不变可知,铜生锈的条件有:水、氧气、二氧化碳,只有①满足条件;图4所示的实验中用氢氧化钠溶液吸收空气中的二氧化碳,结果铜没有生锈,证实二氧化碳也是导致铜生锈的因素之一。
考点:金属活动性的判断、铜生锈条件的探究

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案(7分)化学教师为了调动同学们探究的积极性,布置了一个探究任务:粉笔的成份是初中化学中常见的盐类,请同学们探究粉笔的化学成份。某化学兴趣小组进行了以下探究实验。
【提出猜想】
(1)粉笔的成份氯化物;(2)粉笔的成份碳酸盐;(3)粉笔的成份硫酸盐。
【实验探究】
(1)取一个段白色的粉笔(约1g),在研钵中研成粉末,倒入大烧杯中,加入100mL蒸馏水充分搅拌,静置,发现烧杯底部有较多的白色回体未溶解。根据下表以及后面实验操作现象,判断粉笔的成份属于哪类物质? 。
| 溶解度(20℃) | ﹤0.01g | 0.01g~1g | 1g~10g | ﹥10g |
| 物质分类 | 难溶 | 微溶 | 可溶 | 易溶 |
(3)从烧杯中取少许上层清液注入试管,滴加盐酸溶液,无明显现象产生;
(4)从烧杯中取少许上层清液注入试管,滴加Na2CO3溶液,产生白色沉淀;
(5)从烧杯中取少许上层清液注入试管,滴加BaCl2溶液,产生白色沉淀。
【实验判断】
根据探究实验中出现的现象,请你做出粉笔化学成份可能合理的判断。完成下列填空:
(6)写出粉笔的主要成份化学式 ;
(7)写出【实验探究】(4)中化学反应的化学方程式 ;
(8)写出【实验探究】(5)中化学反应的化学方程式 。
(8分)制作馒头时常加入泡打粉,在制作过程中由于产生二氧化碳气体,使馒头变得松软可口。小明对泡打粉的发面原理产生兴趣,进行了以下实验探究。
【查阅资料】
泡打粉是一种复合膨松剂,又称为发泡粉,可作为快速发面剂用于制作面食。某种泡打粉的主要成分是小苏打粉和酒石酸氢钾。
【提出问题】泡打粉为什么会产生二氧化碳气体?
【猜想】
猜想1:小苏打受热分解产生二氧化碳气体
猜想2:酒石酸氢钾受热分解产生二氧化碳气体
猜想3:小苏打和酒石酸氢钾在溶液中发生反应,产生二氧化碳气体
【实验探究】 小明利用以下实验装置进行探究
装置1 装置2
| 序号 | 实验方案 | 实验现象 | 实验结论 |
| Ⅰ | 在装置1的a试管中放入小苏打,加热 | a试管口内壁有无色液滴,_________。 | b试管中发生反应的化学方程式为______。 猜想1正确 |
| Ⅱ | 在装置1的a试管中放入酒石酸氢钾,加热 | a试管口内壁有无色液滴,石灰水不变浑浊 | ______________ |
| Ⅲ | 在装置2的c试管中放入小苏打和酒石酸氢钾的混合物,滴加________。 | , 石灰水变浑浊 | 猜想3正确 |
(1)通过以上实验探究,小明又查阅到碳酸氢钠分解的反应为: 2NaHCO3
 Na2CO3 + H2O + CO2↑,根据以上实验结论和所学知识,小明对探究问题又提出了第4个猜想,并在以上实验的基础上,利用装置2完成实验验证,其实验方案为____。
Na2CO3 + H2O + CO2↑,根据以上实验结论和所学知识,小明对探究问题又提出了第4个猜想,并在以上实验的基础上,利用装置2完成实验验证,其实验方案为____。(2)通过以上实验探究,下列关于泡打粉的说法中,正确的是_______.
A.泡打粉保存时要注意防潮
B.使用泡打粉前不需要将面进行发酵
C.用纯碱替代泡打粉能起到完全相同的效果
D.泡打粉在加水揉面与蒸馒头的过程中均能起到发面作用
二十一世纪是海洋开发与利用的世纪,我市规划确立了“蓝色经济”发展战略,海洋化学资源的综合利用将是重点发展领域之一。以下是某研究性学习小组在探究海水综合利用中遇到的问题,请你参与解决并填空:
问题一、海水制镁过程中如何富集镁离子?
甲、乙、丙三位同学各自提出自己的设想:
甲:直接往海水中加入石灰乳。
乙:高温加热蒸发海水后,加入石灰乳。
丙:向晒盐后的卤水中,加入石灰乳。
通过分析比较,你认为 ① 的设想最为经济合理(选填“甲”、“乙”或“丙”)。
问题二、粗盐纯化过程中如何除去可溶性杂质?
粗盐中含有硫酸钠、氯化钙等杂质。提纯时,先向粗盐水中加过量的氢氧化钡溶液,目的是完全除尽硫酸钠;再加过量的碳酸钠溶液,除去杂质阳离子;滤去沉淀,向滤液中加入 ② ,将溶液的pH调为7,即得到精盐水。
问题三、海水“制碱” 的产物成分是什么?
同学们从某企业取回少量碳酸氢钠受热完全分解后的固体样品,为确定其成分,进行了如下探究:
【提出猜想】
甲的猜想:样品中只含有碳酸钠;
乙的猜想:样品中含有碳酸钠和氢氧化钠;
丙的猜想:样品中只含有氢氧化钠。
他们做出上述三种猜想的科学依据是 ③ 。
【实验、记录与分析】
| 步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量样品于试管中,加水完全 溶液,再加入过量 ④ | 生成白色沉淀 | 丙的猜想 不成立 |
| 2 | 取步骤1反应后的溶液于试管中 ⑤ | ⑥ | 只有甲的 猜想成立 |
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该小组同学进行如下探究。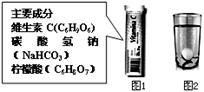
探究一:该气体的成分。
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2。
小明说:不可能含有N2,因为_____________________________。
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO___________________。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
【得出结论】(1)由实验①可知,该气体中肯定含有_________。
(2)由实验②_____________(填“能”或“不能”)确定该气体中不含氧气,理由是_____________________________________________________________。
探究二:维C泡腾片溶液的酸碱性。
向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显_________性。