题目内容
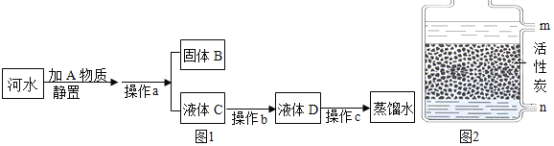
【题目】某化学兴趣小组的同学需要制取一瓶氧气,请与他们一起进行实验之旅
(选择药品)小组同学查阅文献资料,获得了下列信息:过氧化氢、氯酸钾、高锰酸钾等在一定的条件下分解都可以产生氧气。其中过氧化氢溶液价格最低,常温时,在二氧化锰的催化作用下能够迅速分解放出氧气,该过程无副产物;氯酸钾固体价格较高,分解较困难,且常伴有副产物;高锰酸钾固体价格较高,加热即可快速分解。
(1)经讨论,过氧化氢、氯酸钾、高锰酸钾都能产生氧气,是因为______________ (填序号)
①三种方法所需仪器相同 ②反应都需要加热 ③都利用含氧元素化合物分解达到目的
(2)在选择制氧气的原料时,除了要含有所需的元素外,往往还需要考虑_______________等因素(填一条即可)
(明确原理)经过比较,同学们选择过氧化氢作为实验室制取氧气的原料,所发生化学反应的符号表达式为____________。
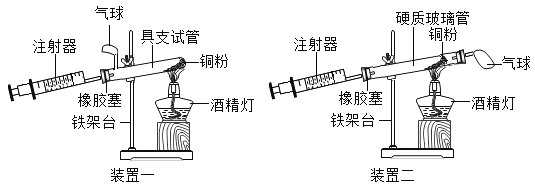
(选择装置)根据下列实验装置图,请回答问题。
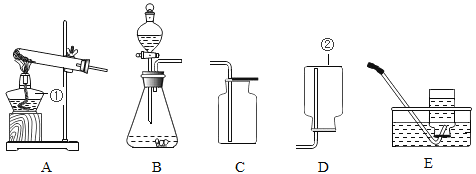
(1)写出上图中标有序号的仪器名称:①_____;②_____。
(2)实验室制取气体时,组装好仪器后,应先___,再添加药品。
(3)实验室用石灰石和稀盐酸制取二氧化碳时,应选用的发生装置是____(选填装置序号)。
(4)利用排空气发收集气体时导管口要接近集气瓶底部,其目的是_________。
(5)因为氧气不易溶于水,所以可以利用装置______(选填装置序号)收集。
(实验方法)“化学反应条件的控制是实验的灵魂”。化学兴小组的同学在老师指导下,进行了“影响过氧化氢溶液分解因素”的探究实验。下表是该小组探究影响过氧化氢分解速率的因素的相关实验数据。请你分析回答:
实验序号 | H2O2溶 液浓度% | H2O2溶液体积/mL | 温度℃ | MnO2的用量/g | 收集氧气的体积/mL | 反应所需 的时间/s |
① | 5 | 1 | 20 | 0.1 | 4 | 17 |
② | 15 | 1 | 20 | 0.1 | 4 | 67 |
③ | 30 | 5 | 35 | 2 | 49 | |
④ | 30 | 5 | 55 | 2 | 11 |
(1)通过实验①和②对比可知,化学反应速率与____________有关;
(2)从实验______和______对比可知,化学反应速率与温度的关系是:__________。
【答案】③ 产物是否污染环境 ![]() 酒精灯 集气瓶 检查装置的气密性 B 排尽瓶内空气,使收集到的气体更纯 E 反应物浓度 ③ ④ 温度越高,反应速率越快
酒精灯 集气瓶 检查装置的气密性 B 排尽瓶内空气,使收集到的气体更纯 E 反应物浓度 ③ ④ 温度越高,反应速率越快
【解析】
[选择药品]
(1)过氧化氢、氯酸钾、高锰酸钾都是利用含氧元素化合物分解达到目的,因此都能产生氧气;故填:③;
(2)在选择制氧气的原料时,除了要含有所需的元素外,往往还需要考虑产物是否污染环境、仪器是否常见、原料是否易得、价格是否便宜等因素;
[明确原理]
在二氧化锰的催化作用下,过氧化氢分解为水和氧气,反应的符号表达式为:![]() ;
;
[选择装置]
(1)仪器①是酒精灯、②是集气瓶;
(2)实验室制取气体时,组装好仪器后,应先检查装置的气密性,再添加药品。
(3)实验室用石灰石和稀盐酸制取二氧化碳时,属于固液常温型,应选用的发生装置是B;
(4)用排空气法收集气体时导管口要接近集气瓶底部,其目的是排尽瓶内空气,使收集到的气体更纯;
(5)因为氧气不易溶于水,所以可以利用排水法来收集;
[实验方法]
(1)实验①和实验②中只有反应物的浓度不同,所以通过实验①和②对比可知,化学反应速率与反应物浓度有关;
(2)实验③和实验④中只有温度不同,从实验③和④对比可知,化学反应速率与温度的关系是:温度越高,反应速率越快;

 名校课堂系列答案
名校课堂系列答案