题目内容
【题目】根据下图的溶解度曲线,完成下列问题:
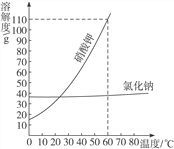
(1)60 ℃时,硝酸钾的溶解度为__________g。在此温度下,往100 g水中加入100 g硝酸钾晶体,充分搅拌后得到的是____________溶液。(填“饱和”或“不饱和”)
(2)下面是两同学分别提出的从海水中获取食盐的方法。
甲:蒸发水 乙:冷却热饱和溶液
你认为_______(填“甲”或“乙”)同学的方法合理。
(3)从图中你还能获得的信息是____________________________。(写一点)
【答案】 110 不饱和 甲 t ℃时硝酸钾和氯化钠的溶解度相等(合理答案均可)
【解析】根据所学知识和图中信息知,(1)60 ℃时,硝酸钾的溶解度为110g,在此温度下,往100g水中加入100g硝酸钾晶体,充分搅拌后得到的是不饱和溶液。(2) 从海水中获取食盐的方法。甲:蒸发水的方法合理,氯化钠溶解度受温度影响不大。(3)从图中你还能获得的信息是t ℃时硝酸钾和氯化钠的溶解度相。
点睛∶溶解度曲线的意义①表示同一种物质在不同温度时的溶解度或溶解度随温度变化的情况;②表示不同物质在同一温度时的溶解度,可以比较同一温度时,不同物质的溶解度的大小。若两种物质的溶解度曲线相交,则在该温度下两种物质的溶解度相等;③根据溶解度曲线可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法;④根据溶解度曲线能进行有关的计算。

 口算能手系列答案
口算能手系列答案【题目】珍珠除了用于制作首饰外,还可制成珍珠粉入药。珍珠的主要成分是碳酸钙。某兴趣小组同学称取11.00g珍珠样品,将120.00g稀盐酸平均分成六次加入(假设珍珠中其它成分不与盐酸反应),测定每次加入稀盐酸充分反应后,产生二氧化碳的总质量如下表所示:
加入稀盐酸的次数 | 1 | 2 | 3 | 4 | 5 | 6 |
加入稀盐酸的质量/g | 20.00 | 20.00 | 20.00 | 20.00 | 20.00 | 20.00 |
充分反应生成二氧化碳的总质量/g | 0.88 | 1.76 | 2.64 | 3.52 | 4.40 | 4.40 |
(1)第6次加入稀盐酸后,产生二氧化碳的质量不继续增加的原因为___________。
(2)计算该珍珠样品中碳酸钙的含量(即珍珠中碳酸钙的质量占珍珠质量的百分数为______,精确到0.1%)
【题目】小苏打(主要成分为NaHCO3)中常含有少量氯化钠。化学兴趣小组的同学为了测定某品牌小苏打中NaHCO3的质量分数,进行了以下实验:称量样品置于烧杯中,向其中慢慢滴加稀盐酸,至不再产生气泡为止,测得的有关数据如下表所示。
物质 | 样品 | 消耗的稀盐酸 | 反应后的溶液 |
质量(g) | 9 | 75.4 | 80 |
试计算(计算结果保留一位小数):
(1)样品中的NaHCO3的质量分数;
(2)所得溶液中NaCl的质量分数。