题目内容
【题目】水和溶液在生产、生活中有着重要的作用。
(1)生活中常用___________的方法降低水的硬度。
(2)下列物质在水中不能形成溶液的是_____________(填序号)。
A 白糖 B 汽油 C 食盐
(3)电解水时,正极上产生的气体具有的性质有__________(填序号)。
A 可以支持燃烧 B 易溶于水 C 作燃料
(4)在配制溶液时,通过计算需要水的体积为 20mL,量取时俯视读数,会导致所配溶液的溶质质量分数__________(填偏大、偏小或无影响)。
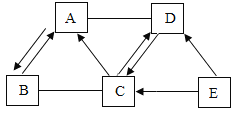
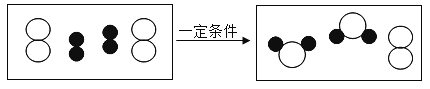
(5)自来水用氯气消毒,其原理是氯气于水反应生成次氯酸(HClO)来消毒,其反应的微观过程可用下图表示:
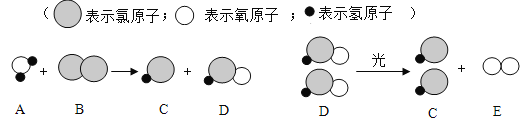
①写出氯气与水反应的化学方程式____________ .
②D 中氯元素的化合价为______.
【答案】煮沸 B A 偏大 ![]() +1
+1
【解析】
(1)生活中常用煮沸的方法降低水的硬度,从而降低水中可溶性钙、镁离子。
(2)白糖、食盐都能形成均一的、稳定的混合物,能够形成溶液;汽油不溶于水,不能形成溶液,得到乳浊液。
故选B。
(3)电解水时,正极上产生的气体是氧气,氧气具有的性质有:可以支持燃烧 ;氧气不易溶于水 ,不能作燃料。故选A。
(4)在配制溶液时,通过计算需要水的体积为 20mL,量取时俯视读数,溶剂偏少会导致所配溶液的溶质质量分数偏大。
(5)①氯气与水反应生成氯化氢和次氯酸,反应的化学方程式为![]()
②D 中氢元素显+1价,氧元素显-2价,氯元素的化合价为+1。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案【题目】铁及其化合物在生活生产中应用非常广泛。
(一)铁材料的有关知识

(1)人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料。这也反映出Cu、Fe、 Al三种金属的活动性由强到弱的顺序是_______________。
(2)磁铁矿是早期司南(如图)的材料,磁铁矿中所含铁的氧化物主要是________________。
(3)我国C919大型客机去年惊艳亮相,客机上大规模使用碳纤维复合材料、铝锂合金、铁钛合金、纳米陶瓷等先进材料,其中不涉及到的材料是_________(选填序号)。
A 合金
B 无机非金属材料
C 合成材料
D 复合材料
(4)铁矿石有赤铁矿、磁铁矿、黄铁矿(FeS2)等。工业上用黄铁矿制取硫酸而不用于炼铁,不用于炼铁原因是:①冶炼中产生SO2污染环境;②______________。
(二)制取碱式硫酸铁
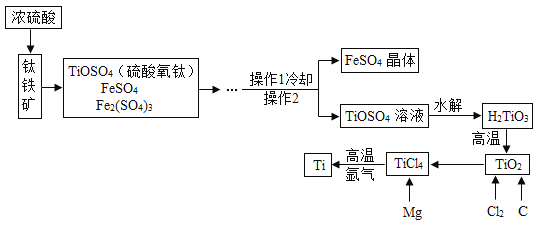
碱式硫酸铁是-种废水处理剂,用硫酸厂的废渣(主要成分为铁的氧化物、少量FeS及SiO2)制备碱式硫酸铁晶体[Fe4(OH)2(SO4)5·6H2O]主要流程如下:

(1)废渣应研磨成粉末,目的是_____。
(2)“酸溶”过程中生成H2S气体的化学方程式为________
(3)过滤后洗涤,证明固体已洗净的方法是_______。
(4)“转化”发生反应的化学方程式为_______,该反应温度不宜过高的原因是________。
(三)碱式硫酸铁晶体的热分解实验
兴趣小组称取此晶体样品25.38g,在科研人员的指导下用下图装置进行热分解实验。
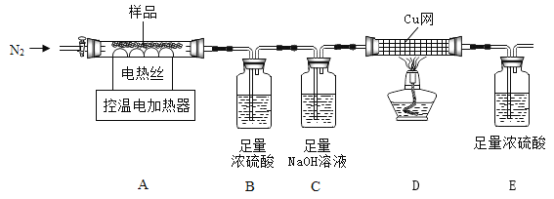
[查阅资料]①碱式硫酸铁晶体(相对分子质量为846)200°C完全分解生成Fe2O3、H2O和Fe2(SO4)3;
②Fe2(SO4)3在500°C完全分解为Fe2O3、SO2、SO3和O2;
③B装置中浓硫酸只能吸收SO3和H2O。.
(1)装配好实验装置后,先要_________。
(2)加热前后及过程中均通入N2,停止加热后继续通N2的目的是防止倒吸和______。
(3)控制不同的温度对A中固体加热,测得装置B、C和D中的质量变化如下表,测得剩余固体质量随温度的变化如图所示。

温度/C | 室温 | 220 | 520 |
B装置/g | 200.00 | 203.78 | 207.78 |
C装置/g | 200.00 | 200.00 | x |
D装置/g | 100.00 | 100.00 | 101.60 |
①如图中m1=____________。
②表格中x=_____________。
③将最终的剩余固体继续加热到更高的温度,发现固体减少0.32g后质量不再改变,写出此过程中发生反应的化学方程式____________。