题目内容
【题目】为探究双氧水浓度对双氧水分解速度的影响。有关实验数据记录如下:
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 待测数据 | |
Ⅰ | 50.0g | 1% | 0.1g | 9 mL |
Ⅱ | 50.0g | 2% | 0.1g | 16 mL |
Ⅲ | x | 4% | 0.1g | 31 mL |
(1)表格中X的值应为________;
(2)待测数据是指_________________________________________________;
(3)从下列仪器中选择合适的装置的并加以组装______________________(填写字母);
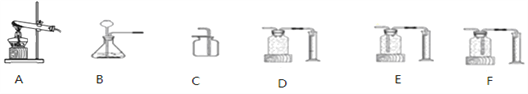
(4)用如图装置进行实验,通过比较______________________也能达到实验目的。
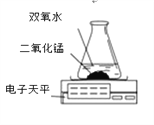
实验结论:在相同条件下,双氧水浓度越大,双氧水分解越快。
【答案】 50.0g 相同时间内产生O2体积 B、F 相同时间电子天平读数差值大小(表述合理即可)
【解析】(1)为探究双氧水浓度对双氧水分解速度的影响,应采用控制变量法,即过氧化氢的浓度不同,其他条件要完全相同,故表格中X的数值为50.0g;(2)探究双氧水浓度对双氧水分解速度可通过比较相同时间内产生O2体积即可,即待测数据是相同时间内产生O2体积;(3)根据反应物的状态和反应条件选择发生装置,用过氧化氢溶液和二氧化锰为原料制取氧气,属于固液体常温下的反应,故选B作为发生装置;要测定氧气的气体,那么可采用排水法收集,选F装置,排出的水的体积即为生成的氧气的体积;(4)过氧化氢分解生成水和氧气,氧气是气体,会逸散到空气中,故可比较相同时间电子天平读数差值大小,差值越大,说明反应速率越快。

练习册系列答案
相关题目