题目内容
【题目】某课外活动小组设计了测定空气中氧气含量的实验,装置如图所示,回答下列问题:
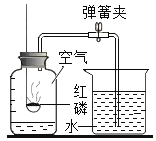
(1)反应后瓶中剩余的气体的一条物理性质是_____
(2)已知金属镁会与空气中的氧气和氮气反应,反应后产物皆为固体。 如果用镁条代替红磷进行此实验,则进入集气瓶中的水会_____(填“更多”“不变”或“更少”)。
(3)小华同学利用该装置测定空气中氧气的含量,打开止水夹发现进入集气瓶中水的体积小于集气瓶内空气总体积的![]() ,可能的原因是_____(填字母代号)
,可能的原因是_____(填字母代号)
A 实验前没有将止水夹夹紧
B 实验装置可能漏气
C 实验中所取的红磷过量
D 实验中所取的红磷不足
E 红磷点燃后伸入集气瓶未立即塞紧橡胶塞
F 未等装置完全冷却就打开止水夹读数
【答案】不溶于水 更多 BDF
【解析】
(1)反应后瓶中剩余的气体的物理性质是不溶于水等。
(2)如果用镁条代替红磷进行此实验,镁即消耗氧气,又消耗氮气,则进入集气瓶中的水会更多。
(3)A.实验前没有将止水夹夹紧,会导致集气瓶中部分气体膨胀通过导管逸出,从而导致实验结果偏大,即进入集气瓶中的水的体积大于集气瓶中空气总体积的五分之一;
B.实验装置可能漏气,导致进入集气瓶中的水的体积小于集气瓶中空气总体积的五分之一;
C.实验中所取的红磷过量,不影响实验结果;
D.实验中所取的红磷不足,导致进入集气瓶中的水的体积小于集气瓶中空气总体积的五分之一;
E.红磷点燃后伸人集气瓶未立即塞紧橡胶塞,会导致集气瓶中部分气体膨胀逸出,从而导致实验结果偏大,即进入集气瓶中的水的体积大于集气瓶中空气总体积的五分之一;
F.未等装置完全冷却就打开止水夹读数,会导致进入集气瓶中的水的体积小于集气瓶中空气总体积的五分之一。
故填:不溶于水;更多;BDF。

 字词句段篇系列答案
字词句段篇系列答案【题目】被称为“绿色氧化剂”的过氧化氢(![]() ),俗称双氧水,是一种无色液体,常用作氧化剂、消毒杀菌剂和漂白剂等。在较低温度下和少量催化剂(如
),俗称双氧水,是一种无色液体,常用作氧化剂、消毒杀菌剂和漂白剂等。在较低温度下和少量催化剂(如![]() )条件下,它能迅速分解,生成氧气和水。请回答下列问题:
)条件下,它能迅速分解,生成氧气和水。请回答下列问题:
小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题他设计并完成了下表所示的探究实验:
(1)请你帮小丽同学填写上表中未填完的空格。
实验操作 | 实验现象 | 实验结论或总结 | ||
结论 | 总结 | |||
实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有少量气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是_____. 反应的文字表达式为:_____. | 二氧化锰是过氧化氢分解的催化剂 |
实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | _____ | |
实验三 | _____ | _____ | 二氧化锰能加快过氧化氢的分解 | |
(2)在小丽的探究实验中,“实验一”和“实验二”起的作用是_____。
【题目】按要求填写下列表格:
实验内容 | 反应的文字表达式 | 简答 |
硫在空气中燃烧 | _____ | 该反应火焰的颜色为_____色。 |
加热高锰酸钾制氧气 | _____ | 该反应中试管口略向下倾斜的原因是:_____。 |
铁丝在氧气中的燃烧 | _____ | 该实验中,集气瓶底要放点水或细沙的原因是_____。 |
加热氯酸钾和二氧化锰混合物制取氧气 | _____ | 二氧化锰在反应前后没有改变是_____。 |
过氧化氢制取氧气 | _____ | 反应的基本类型是:_____反应 |
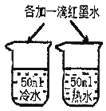
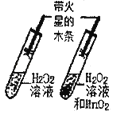
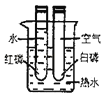
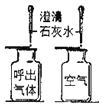
【题目】对比实验是实验探究的重要方法,下列对比实验设计不能实现相应实验目的是( )
实验设计 |
|
|
|
|
选项 | A探究温度对分子运动快慢的影响 | B探究MnO2能否加H2O2分解 | C.探究空气是燃烧的必要条件 | D.探究空气、呼出气体中CO2含量 |
A. A B. B C. C D. D