题目内容
【题目】按要求填写下列表格:
实验内容 | 反应的文字表达式 | 简答 |
硫在空气中燃烧 | _____ | 该反应火焰的颜色为_____色。 |
加热高锰酸钾制氧气 | _____ | 该反应中试管口略向下倾斜的原因是:_____。 |
铁丝在氧气中的燃烧 | _____ | 该实验中,集气瓶底要放点水或细沙的原因是_____。 |
加热氯酸钾和二氧化锰混合物制取氧气 | _____ | 二氧化锰在反应前后没有改变是_____。 |
过氧化氢制取氧气 | _____ | 反应的基本类型是:_____反应 |
【答案】硫+氧气![]() 二氧化硫 淡蓝色 高锰酸钾
二氧化硫 淡蓝色 高锰酸钾![]() 锰酸钾+二氧化锰+氧气 防止水蒸气冷凝形成的水掉落试管中使试管炸裂 铁+氧气
锰酸钾+二氧化锰+氧气 防止水蒸气冷凝形成的水掉落试管中使试管炸裂 铁+氧气![]() 四氧化三铁 防止高温融熔物掉落瓶底使瓶底炸裂 氯酸钾
四氧化三铁 防止高温融熔物掉落瓶底使瓶底炸裂 氯酸钾![]() 氯化钾+氧气 质量和化学性质 过氧化氢
氯化钾+氧气 质量和化学性质 过氧化氢![]() 水+氧气 分解反应
水+氧气 分解反应
【解析】
硫在空气中燃烧,火焰为淡蓝色,生成有刺激性气味的气体,硫与氧气在点燃条件下生成二氧化硫,反应的文字表达式为:硫+氧气![]() 二氧化硫;
二氧化硫;
加热高锰酸钾制氧气,高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰和氧气,反应的文字表达式为:高锰酸钾![]() 锰酸钾+二氧化锰+氧气,反应中试管口略向下倾斜的原因是防止水蒸气冷凝形成的水掉落试管中使试管炸裂;
锰酸钾+二氧化锰+氧气,反应中试管口略向下倾斜的原因是防止水蒸气冷凝形成的水掉落试管中使试管炸裂;
铁丝在氧气中的燃烧,铁与氧气在点燃条件下生成四氧化三铁,反应的文字表达式为:铁+氧气![]() 四氧化三铁,该实验中,集气瓶底要放点水或细沙的原因是防止高温融熔物掉落瓶底使瓶底炸裂;
四氧化三铁,该实验中,集气瓶底要放点水或细沙的原因是防止高温融熔物掉落瓶底使瓶底炸裂;
加热氯酸钾和二氧化锰混合物制取氧气,氯酸钾在二氧化锰做催化剂的条件下受热分解生成氯化钾和氧气,反应的文字表达式为:氯酸钾![]() 氯化钾+氧气,二氧化锰做催化剂,在反应前后质量和化学性质不发生改变;
氯化钾+氧气,二氧化锰做催化剂,在反应前后质量和化学性质不发生改变;
过氧化氢制取氧气,过氧化氢在二氧化锰做催化剂的条件下分解生成水和氧气,反应的文字表达式为:过氧化氢![]() 水+氧气,反应的基本类型是分解反应。
水+氧气,反应的基本类型是分解反应。

【题目】某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(图1)。
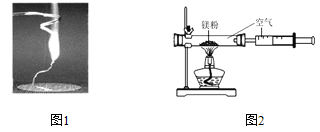
(1)镁跟氧气反应的化学方程式是_____________。
(2)小明通过称量发现:图1中石棉网上收集到产物的质量小于镁条的质量。你认为其原因可能是_______________。
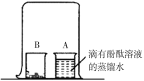
(3)小红按图2装置改进实验,验证质量守恒定律,她却发现产物中还有一些黄色固体。
(提出问题)黄色固体是什么呢?
(查阅资料)①氧化镁为白色固体;
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水反应生成氨气,氨气能使酚酞溶液变红。
(做出猜想)黄色固体为Mg3N2。
(实验探究)
实验操作 | 实验现象及结论 |
| 现象:_________。 结论:燃烧产物中含Mg3N2 |
(反思与交流)①为什么在发生化学反应前后各物质的质量总和相等?请从微观角度解释_______。
②空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,为什么呢?请给出合理的解释_______。
(拓展延伸)①如果用图2装置(气密性良好)和药品(足量)测定空气中氧气含量,该实验所测得的氧气体积分数_______(填“大于”、“小于”或“等于”) 1/5。
②2.40g镁条在某氧气和氮气的混合气中完全燃烧,所得固体质量可能是___。
A 3.33g B 4.00g C 3.28g D 3.96g