题目内容
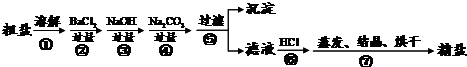
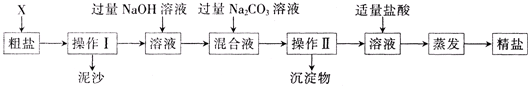
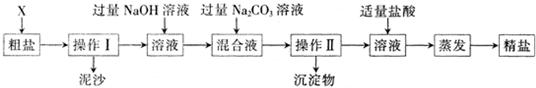
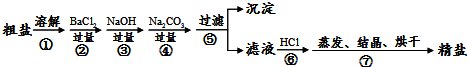
通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质.以下是制备精盐的实验方案,各步操作流程如下:

(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是________.
(2)第②步操作加入过量的BaCl2目的是除去粗盐中的________(填化学式),写出这个反应的化学方程式________.
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、CaCO3、BaCO3________(填化学式).
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是________.
(5)在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是________.
解:(1)用玻璃棒搅拌,加速了液体的流动,使固体很快溶解;
(2)加入过量的氯化钡,氯离子对氯化钠来说不是杂质,钡离子可以将硫酸根离子转化为沉淀,第②步操作加入过量的BaCl2目的是除去粗盐中的硫酸钠,反应的化学方程式Na2SO4+BaCl2=BaSO4↓+2NaCl;
(3)第二步后溶液中剩下没有反应的氯化钡,第四步加入碳酸钠,除了将氯化钙沉淀以外,还可以除去过量的氯化钡,故第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、CaCO3、BaCO3、Mg(OH)2;
(4)氢氧化钾会与氯化镁反应生成氢氧化镁沉淀和氯化钾,氯化钾对氯化钠来说就是杂质了,在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是会引入新的杂质氯化钾;
(5)最后得到的滤液中溶质除含有氯化钠外还含有碳酸钠和氢氧化钠,利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是除去多余的氢氧化钠和碳酸钠.
故答案为:(1)加快粗盐溶解; (2)Na2SO4;Na2SO4+BaCl2=BaSO4↓+2NaCl;(3)Mg(OH)2;(4)会引进新的杂质KCl;(5)除去多余的氢氧化钠和碳酸钠.
分析:(1)可以从粗盐溶解过程中的玻璃棒的作用分析.
(2)从加入的物质中的离子角度分析.
(3)从④步前的溶液中的离子角度分析.
(4)可以从复分解反应得原理以及加入的物质引入的离子角度分析.
(5)根据滤液中溶质含有碳酸钠和氢氧化钠进行解答.
点评:本题主要考查了粗盐提纯过程中的除杂方面的知识,综合性强,双基要求高.
(2)加入过量的氯化钡,氯离子对氯化钠来说不是杂质,钡离子可以将硫酸根离子转化为沉淀,第②步操作加入过量的BaCl2目的是除去粗盐中的硫酸钠,反应的化学方程式Na2SO4+BaCl2=BaSO4↓+2NaCl;
(3)第二步后溶液中剩下没有反应的氯化钡,第四步加入碳酸钠,除了将氯化钙沉淀以外,还可以除去过量的氯化钡,故第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、CaCO3、BaCO3、Mg(OH)2;
(4)氢氧化钾会与氯化镁反应生成氢氧化镁沉淀和氯化钾,氯化钾对氯化钠来说就是杂质了,在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是会引入新的杂质氯化钾;
(5)最后得到的滤液中溶质除含有氯化钠外还含有碳酸钠和氢氧化钠,利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是除去多余的氢氧化钠和碳酸钠.
故答案为:(1)加快粗盐溶解; (2)Na2SO4;Na2SO4+BaCl2=BaSO4↓+2NaCl;(3)Mg(OH)2;(4)会引进新的杂质KCl;(5)除去多余的氢氧化钠和碳酸钠.
分析:(1)可以从粗盐溶解过程中的玻璃棒的作用分析.
(2)从加入的物质中的离子角度分析.
(3)从④步前的溶液中的离子角度分析.
(4)可以从复分解反应得原理以及加入的物质引入的离子角度分析.
(5)根据滤液中溶质含有碳酸钠和氢氧化钠进行解答.
点评:本题主要考查了粗盐提纯过程中的除杂方面的知识,综合性强,双基要求高.

练习册系列答案
相关题目
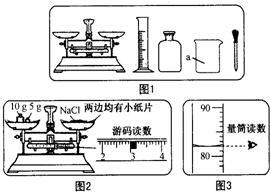 某实验小组利用图1所示仪器进行“配制质量分数一定的氯化钠溶液”的实验:
某实验小组利用图1所示仪器进行“配制质量分数一定的氯化钠溶液”的实验: