题目内容
9.右图是某化工厂生产的产品包装袋上的标签.| 碳酸氢铵 化学式:NH4HCO3 含氮量:16.8% 纯度:95% 净重:50 kg |
(2)计算碳酸氢铵的相对分子质量
(3)某农民李大伯需向自己的责任田中追施氮元素8.4kg;需这种氮肥多少千克?
(4)通过计算判断此产品是否是合格产品?
分析 (1)根据1个碳酸氢铵分子的构成,进行分析解答;
(2)根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行分析解答;
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答;
(4)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,判断此产品是否合格;
解答 解:(1)1个碳酸氢铵分子是由1个氮原子、5个氢原子、1个碳原子和3个氧原子构成的,则碳酸氢铵中氮、氢、碳、氧四种原子的个数比为1:5:1:3.
(2)碳酸氢铵的相对分子质量为:14+1×4+1+12+16×3=79.
(3)某农民李大伯需向自己的责任田中追施氮元素8.4kg;需这种氮肥的质量为8.4kg÷($\frac{14}{79}$×100%)=47.4kg;
(4)纯净的碳酸氢铵中氮元素的质量分数为$\frac{14}{79}$×100%=17.7%,此产品中氮元素的质量分数为:17.7%×95%═16.815%,故为合格产品.
故答案为:(1)1:5:1:3;(2)79;(3)47.4kg;(4)合格.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
18.下列关于溶液组成的说法正确的是( )
| A. | 溶质一定是固体 | |
| B. | 溶剂一定是水 | |
| C. | 溶液一定是混合物 | |
| D. | 溶液的体积等于溶质与溶剂的体积之和 |
 A、B、C、D、E是常见的五种无色气体,X、Y、Z是化合物.它们之间的转化关系如图所示(图中略去部分反应产物),其中反应⑤是实验室制气体E的常用方法.
A、B、C、D、E是常见的五种无色气体,X、Y、Z是化合物.它们之间的转化关系如图所示(图中略去部分反应产物),其中反应⑤是实验室制气体E的常用方法.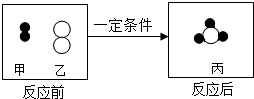 物质都是由粒子构成的,化学反应的实质是粒子之间的重新组合.如图为甲、乙两种不同的气态物质在一定条件下反应生成丙物质的微观示意图.其中其中●和○分别表示氢原子和氮原子,请据图回答:
物质都是由粒子构成的,化学反应的实质是粒子之间的重新组合.如图为甲、乙两种不同的气态物质在一定条件下反应生成丙物质的微观示意图.其中其中●和○分别表示氢原子和氮原子,请据图回答: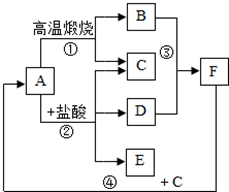 A、B、C、D、E、F为初中化学常见物质,它们之间的转化如图所示,A是固体物质,C是气体,请回答下列问题:
A、B、C、D、E、F为初中化学常见物质,它们之间的转化如图所示,A是固体物质,C是气体,请回答下列问题: