题目内容
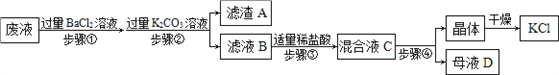
【题目】同学们完成实验后留下的废液中含有K2CO3、KCl和Na2SO4三种物质,在老师的指导下,化学小组的同学设计以下流程回收KCl晶体。
请回答:
(1)步骤①反应的化学方程式____________________、______________________。
(2)步骤②加入过量K2CO3溶液的目的是____________________________________;滤液B中的溶质是_______________、_____________、_______________(写化学式)。
(3)步骤③判断盐酸适量的现象是_________________________________________。
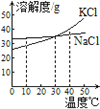
(4)混合液C中的溶质是KCl和NaCl,观察溶解度曲线,步骤④所包含的具体操作是______、降温结晶、过滤。降温结晶的最佳温度范围是________℃以下,晶体表面的杂质最好用______________________进行洗涤。
【答案】 K2CO3+BaCl2==BaCO3↓+2KCl Na2SO4+BaCl2==BaSO4↓+2NaCl 除去过量的BaCl2 KCl NaCl K2CO3 刚好不再有气泡冒出 蒸发浓缩 30 饱和KCl溶液
【解析】(1)步骤①加入过量的氯化钡溶液,氯化钡与碳酸钾反应生成碳酸钡和氯化钾,反应的化学方程式为:K2CO3+BaCl2==BaCO3↓+2KCl;氯化钡与硫酸钠反应生成硫酸钡和氯化钠,反应的化学方程式为:Na2SO4+BaCl2==BaSO4↓+2NaCl;
(2)加入过量K2CO3溶液的目的是除去过量的BaCl2,反应生成碳酸钡和氯化钾,所以液B中的溶质是氯化钾、氯化钠和过量的碳酸钾;
(3)步骤③加入盐酸与碳酸钾反应生成氯化钾、水和二氧化碳气体,所以盐酸适量的现象是刚好不再有气泡冒出;
(4)由于氯化钾溶解度随温度升高而增大,氯化钠的溶解度几乎不受温度的影响,所以要分离氯化钠和氯化钾可以蒸发浓缩形成热饱和溶液,降温结晶、过滤。由于氯化钾的溶解度在30℃以下比氯化钠小,酸钠的溶解度受温度影响比氯化钠大,降温的过程中会析出大量的氯化钾,所以,降温结晶的最佳温度范围是30℃以下;为防止氯化钾的溶解,晶体表面的杂质最好用饱和KCl溶液进行洗涤。

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案【题目】小明在探究CO2和NaOH是否发生反应时,设计出下列三种装置进行实验:
请回答以下几个问题:

(1)以上三个实验中,①③有明显现象,请你帮小明记录他观察到的实验现象:
实验①_________________。实验③_________________。
(2)实验②因选用仪器不当导致未能观察到明显现象,请你帮小明寻找一种物品替代该装置中的广口瓶,以使实验取得成功,你将选用的物品是________________,改进后能看到的实验现象是______________________。
(3)请你进一步设计实验来检验CO2和NaOH溶液反应生成了Na2CO3,并将有关的实验操作、现象、结论填入下表:
实验操作 | 实验现象 | 结 论 |
___________________ | ________________ | ________________ |