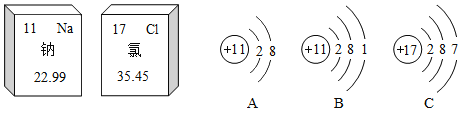
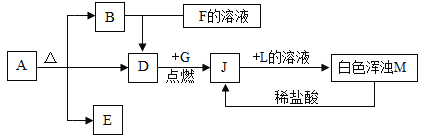
题目内容
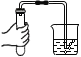
【题目】现有下列实验装置图,回答问题:
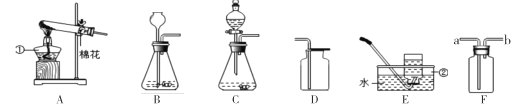
(1)写出图中标有序号的仪器名称:①___________,②________。
(2)选用A装置来制取氧气,其反应的化学方程式为____________,能用D装置收集氧气的原因是___________。
(3)实验室制取二氧化碳,其反应的化学方程式为_____________,若用F装置来收集,验满时应将燃着的木条放在_________(填“a”或“b”)端管口,看到___________,则说明已收集满。
(4)实验室在常温下用块状电石与水反应,制取不易溶于水的乙炔(C2H2)气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂。要制取较纯净的乙炔气体你认为图中最适合的发生和收集装置为________(填序号)。
【答案】酒精灯 水槽 ![]() 氧气的密度比空气大
氧气的密度比空气大  b 木条熄灭 CE
b 木条熄灭 CE
【解析】
(1)据图可知仪器①是酒精灯,②是水槽;
(2 A装置可以用于加热高锰酸钾来制取氧气,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,其反应的化学方程式为![]() ,氧气的密度比空气的密度大,因此能用向上排空气法收集;
,氧气的密度比空气的密度大,因此能用向上排空气法收集;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,,其反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;若用F装置来收集,验满时应将燃着的木条放在b端管口,看到木条熄灭;
(4)实验室在常温下用块状电石与水反应制取不易溶于水的乙炔(C2H2)气体,该反应必须严格控制加水速度,因此选用C;要制取较纯净的乙炔气体,应该用排水法收集。要制取较纯净的乙炔气体你认为图中最适合的发生和收集装置为CE。

 互动英语系列答案
互动英语系列答案【题目】下面是小婷同学测定黄铜(铜锌合金)中铜的质量分数的过程。小婷同学取10 g黄铜于烧杯中,将120 g稀硫酸分六次加入烧杯中,测得加入的稀硫酸质量和烧杯中剩余物的质量如下表:
次数 | 一 | 二 | 三 | 四 | 五 | 六 |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量/g | 29.96 | 49.92 | m | 89.84 | 109.8 | 129.8 |
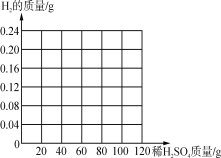
①10g黄铜完全反应产生H2的质量________g;
②表中m=________;
③求黄铜中铜的质量分数________ (写出计算过程)。
④请在如图画出10g黄铜加入稀硫酸与生成氢气的质量的图象________。