题目内容
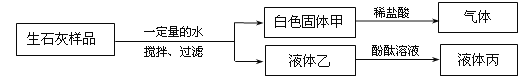
【题目】钓鱼岛及其附属海域是我国固有领土,蕴藏着丰富的海洋资源。从海水中制备纯碱和金属镁的流程如图所示:
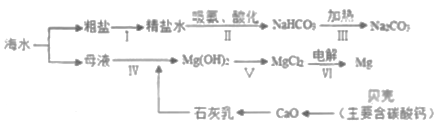
回答下列问题:
(1)由氧化钙得到石灰乳的基本反应类型为______。
(2)步骤V中所加试剂是______。
(3)粗盐水中主要含有CaCl2、MgSO4等可溶性余质,可加入下列物质,利用过滤等操作进行除杂。则加入下列三种物质的先后顺序为______(填序号)。
①适量稀盐酸 ②过量的碳酸钠溶液 ③过量的氢氧化钡溶液
【答案】化合反应 稀盐酸 ③②①
【解析】
(1)氧化钙与水反应生成氢氧化钙,该反应是由两种物质生成一种物质,属于化合反应;
(2)步骤Ⅴ中是氢氧化镁转化为氯化镁,氢氧化镁与盐酸反应生成氯化镁和水,故所加试剂是稀盐酸;
(3)粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,氯化钙与碳酸钠反应生成碳酸钙沉淀和氯化钠,除去氯化钙可以加入碳酸钠溶液;硫酸镁与氢氧化钡反应生成氢氧化镁沉淀和氢氧化钠,除去硫酸镁可以加入氢氧化钡溶液;碳酸钠与氢氧化钡反应生成氢氧化钠和碳酸钡,碳酸钠溶液可除去过量的氢氧化钡,碳酸钠应该加在氢氧化钡的后面;碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,氢氧化钠与盐酸反应生成氯化钠和水,适量的盐酸可除去过量的碳酸钠和生成的氢氧化钠,则加入下列三种物质的先后顺序为③②①。

【题目】厨师在厨房炒菜时加了料后再加醋,就让菜肴变得香美可口,这其实隐藏了一个化学的小秘密:醋中的乙酸与料酒中的乙醇反应生成了有香味的乙酸乙酯,下表中是几种常见的酯,请完成下列问题:
酯的名称 | 甲酸甲酯 | 乙酸乙酯 | 丙酸丙酯 | 丁酸丁酯 |
化学式 | C2H4O2 | C4H8O2 | C6H12O2 | X |
(1)甲酸甲酯中碳元素、氢元素、氟元素的质量比为_____,其中氢元素的质量分数为_____;(保留0.1%)
(2)比较归纳是学习的重要方法,根据表推测X的化学式是_____;
(3)丙酸丙酯中氧元素的质量分数_____(填“大于”、“小于”或“等于”)丁酸丁酯中氧元素的质量分数;
(4)若菜肴中的乙酸乙酯在人体内代谢时其中的碳元素完全部转化为CO2,则44mg的乙酸乙酯完全代谢产生的CO2的质量为多少?(请写出计算过程)_________