题目内容
【题目】已知 CuS、Cu2S 粉末的颜色和 CuO 相似,且都不溶解于水。在空气中煅烧时,CuS 和Cu2S 都转化成 CuO 和 SO2。
(1)请写出 CuS、Cu2S 在空气中煅烧时发生反应的化学方程式:________、________。
(2)根据叙述,设计一个不用其他化学试剂鉴别 CuO、CuS、Cu2S三种粉末的实验方案(写明步骤与结论)________。
【答案】![]()
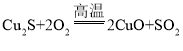
实验步骤 | 实验现象 | 结论 |
1.分别称取相同质量的样品,在空气中燃烧 | 有一种固体无变化,两种固体产生刺激性气味气体 | 固体无变化的是氧化铜,产生刺激性气味气体的是硫化铜和硫化亚铜 |
2.分别称量硫化铜和硫化亚铜灼烧后剩余物质的质量 | 有一种样品质量减轻,一种样品质量不变 | 质量减轻的是硫化铜,质量不变的是硫化亚铜 |
【解析】
(1)CuS、Cu2S 在空气中煅烧,与氧气反应,均生产氧化铜和二氧化硫,发生反应的化学方程式分别为:![]() 、
、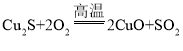 。
。
(2)由![]() 、
、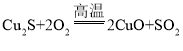 可知,CuS、Cu2S 在空气中煅烧均有刺激性气味气体生成,CuS煅烧后质量减小,Cu2S煅烧后质量不变,故可设计实验:
可知,CuS、Cu2S 在空气中煅烧均有刺激性气味气体生成,CuS煅烧后质量减小,Cu2S煅烧后质量不变,故可设计实验:
实验步骤 | 实验现象 | 结论 |
1.分别称取相同质量的样品,在空气中燃烧 | 有一种固体无变化,两种固体产生刺激性气味气体 | 固体无变化的是氧化铜,产生刺激性气味气体的是硫化铜和硫化亚铜 |
2.分别称量硫化铜和硫化亚铜灼烧后剩余物质的质量 | 有一种样品质量减轻,一种样品质量不变 | 质量减轻的是硫化铜,质量不变的是硫化亚铜 |

【题目】工业上冶炼金属锌主要有火法和湿法两种工艺。
(1)火法炼锌时发生如下反应:
2ZnS+3O2 2ZnO+2SO2;2C+O2
2ZnO+2SO2;2C+O2 2CO;ZnO+CO
2CO;ZnO+CO Zn+CO2。
Zn+CO2。
①化合物ZnS中Zn元素的化合价是_____,上述反应在鼓风炉中控制温度在1100℃至1300℃进行,使生成的锌气化蒸馏出来,蒸馏过程属于_____变化。
②已知反应前矿石中ZnS的质量为ag,则理论上可以生成Zn的质量为_____g(用含a的式子表示,可不化简)。
(2)湿法炼锌的原理是利用CO32-与Zn2+结合生成ZnCO3沉淀。某研究小组利用该原理,用碳酸钠作为沉淀剂,探究从含锌废水中回收锌的最佳条件,实验的数据如下:
实验编号 | 初步处理的废液用量/mL | pH值 | 反应时间/min | 沉锌率% |
a | 800 | 6 | 30 | 84.30 |
b | 800 | 7.5 | 10 | 85.27 |
c | 800 | 7.5 | 30 | 99.60 |
d | 800 | 8.0 | 30 | 99.55 |
①本实验探究了哪些因素对沉锌率的影响_____。
②已知碳酸钠溶液呈碱性。实验中碳酸钠使用量最大的是_____(填编号)。工业生产中采用实验_____(填编号)的提取条件更合理。