题目内容
【题目】某校兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中(如下图),有一装溶液的试剂瓶未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究:
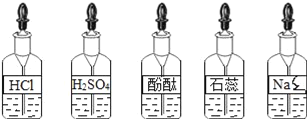
(提出问题)这瓶溶液是什么溶液?
(获得信息)酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
(提出猜想)这瓶溶液是:猜想一:氯化钠溶液;猜想二:氢氧化钠溶液;猜想三:碳酸钠溶液。
(实验推断)
(1)小丽取样滴加无酚酞试液,溶液呈红色,得出结论:该溶液不可能是______溶液,理由是________;
(2)小刚另取样滴加稀盐酸有______产生,反应的化学方程式为______,小刚得出结论:该溶液是碳酸钠溶液。
(3)小青认为小刚的结论不完全正确,理由是_______。
小组同学讨论后一致认为还需要进行如下实验:
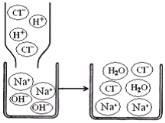
(继续探究)另取样加入过量的CaCl2溶液,观察到有______产生,设计这一步骤的目的是_______;该反应的化学方程式为________静置后,取上层清液,滴入酚酞试液,溶液呈红色。
(实验结论)这瓶溶液是_________。
(探究启示)实验取完药品后应________。
【答案】氯化钠 氯化钠溶液呈中性,不能使酚酞试液变色 气泡 Na2CO3 + 2HCl = 2NaCl+ H2O + CO2↑ 露置于空气中的NaOH溶液与空气中的CO2反应也生成碳酸钠 白色沉淀 完全除去Na2CO3避免其对NaOH性质的影响,或完全除去溶液中的CO32-,避免其对OH-检验造成干扰 CaCl2+ Na2CO3 = CaCO3↓+2NaCl NaOH溶液(填变质的NaOH溶液也可) 立即盖好瓶盖
【解析】
解答本题首先分析实验目的,实验目的是对敞口放置在空气中的某钠的化合物进行探究。其次要认真分析假设中氯化钠、氢氧化钠、碳酸钠的化学性质,结合实验现象进行综合分析。最后在完成解答时要针对具体的知识点的答题要求进行,避免出现知识性错误。可通过滴加酚酞来证明氯化钠的存在与否,加盐酸出现气体,不能证明就是碳酸钠,因为题意中是敞口容器,若是氢氧化钠可能变质生成部分碳酸钠。
(1)小丽取样滴加无酚酞试液,溶液呈红色,得出结论:该溶液不可能是氯化钠溶液,理由:氯化钠溶液显中性,不能使酚酞试液变色。故填:氯化钠;氯化钠溶液显中性,不能使酚酞试液变色。
(2)小刚另取样滴加稀盐酸有气泡产生,是因为碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑。故填:气泡;Na2CO3+2HCl═2NaCl+H2O+CO2↑。
(3)小青认为小刚的结论不完全正确,理由是露置于空气中的NaOH溶液与空气中的CO2反应也生成碳酸钠。故填:露置于空气中的NaOH溶液与空气中的CO2反应也生成碳酸钠。
[继续探究]另取样加入过量的CaCl2溶液,观察到有白色沉淀产生,是因为碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,设计这一步骤的目的是完全除去Na2CO3避免其对NaOH性质的影响,或完全除去溶液中的CO32-,避免其对OH-检验造成干扰;该反应的化学方程式为:CaCl2+ Na2CO3 = CaCO3↓+2NaCl,静置后,取上层清液,滴入酚酞试液,溶液呈红色,说明溶液中含有氢氧化钠。故填:白色沉淀;完全除去Na2CO3避免其对NaOH性质的影响,或完全除去溶液中的CO32-,避免其对OH-检验造成干扰;CaCl2+ Na2CO3 = CaCO3↓+2NaCl。
[实验结论]这瓶溶液是氢氧化钠溶液,已经部分变质。故填:氢氧化钠溶液(填变质的NaOH溶液也可)。
[探究启示]实验取完药品后应立即盖好瓶塞。故填:立即盖好瓶塞。

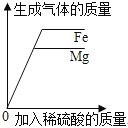
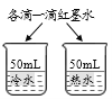
【题目】控制变量是实验探究的重要方法。下列实验设计不能达到实验目的的是( )
|
|
|
|
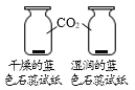
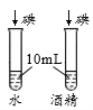
A.探究铁、镁金属活动性强弱 | B.探究二氧化碳与水是否发生反应 | C.探究不同溶剂中物质溶解性大小 | D.探究温度对分子运动快慢的影响 |
A. AB. BC. CD. D