题目内容
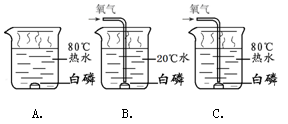
【题目】(7分)某化学兴趣小组根据以下图示进行模拟炼铁的实验,并对产物成分及含量进行探究。
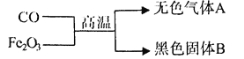
【提出问题】无色气体A有哪些成分?黑色固体B可能是什么?
【查阅资料】(1)常温下,一氧化碳能与氯化钯(PdCl2)溶液反应生成钯(不溶于水)、 二氯化碳和氯化氧。
(2)铁的氧化物都能与稀盐酸、稀硫酸反应,其中氧化铁为红棕色,其余都为黑色,并且只有四氧化三铁能被磁铁吸引。
【提出猜想】猜想1:无色气体A一定是C02,原因是 (用化学方程式表示)。
猜想2:黑色固体B全部是铁。
【交流与讨论】小华认为猜想1不一定正确,无色气体中除了CO2外,可能含有CO。
【探究反思】(1)为验证小华的衍箍l,大家按以下图示进行实验,过程与现象如下:
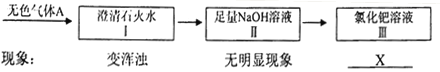
①当X现象为 时,可以确定猜想1是错误的,写出产生该现象的化学方程式: 。
②Ⅱ中无明显现象,但可以往Ⅱ中滴加足量 (填试剂名称或化学式)证明气体在Ⅱ中确实已发生了反应。
(2)为验证猜想2,大家称取7g黑色固体B,按以下图示进行实验探究,过程与现象如下:
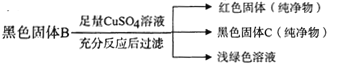
①经过分析,大家确定猜想2是错误的,理由是 。
②为了进一步确定黑色固体C的成分,你的方法是 (写出实验操作、现象及结论)。
③实验结束后,称得红色固体的质量为6.4g,则黑色固体B中铁单质的质量分数为 。
【答案】 【提出猜想】猜想1:3CO+ Fe2O3 高温 2Fe + 3CO2【探究反思】(1)①沉淀产生;H2O+CO+PdCl2=Pd↑+CO2+2HCl ②氯化钙溶液;(2)①铁和足量硫酸铜反应生成硫酸亚铁和铜,不能产生黑色固体.;②实验操作:把磁铁靠近黑色固体;实验现象:黑色固体被吸引;实验结论:黑色固体是四氧化三铁.③80%
【解析】
试题分析:【提出猜想】猜想1:无色气体A一定是C02,原因是:氧化铁和一氧化碳反应生成二氧化碳,反应的化学方程式为:3CO+ Fe2O3 高温 2Fe + 3CO2 【探究反思】(1)①当X现象为产生黑色沉淀时,可以确定猜想1是错误的,产生该现象的化学方程式为:H2O+CO+PdCl2=Pd↓+CO2+2HCl②Ⅱ中无明显
现象,但可以往Ⅱ中滴加足量CaCl2证明气体在Ⅱ中确实已发生了反应,因为氯化钙能和二氧化碳与氢氧化钠反应生成的碳酸钠反应生成白色沉淀--碳酸钙.(2)①经过分析,大家确定猜想2是错误的,理由是:铁和足量硫酸铜反应生成硫酸亚铁和铜,不能产生黑色固体.②为了进一步确定黑色固体C的成分,实验方法是:实验操作:把磁铁靠近黑色固体;实验现象:黑色固体被吸引;实验结论:黑色固体是四氧化三铁.实验操作:把适量黑色固体置于试管中,加入适量的稀硫酸;实验现象:溶液变成浅绿色;实验结论:黑色固体是氧化亚铁.实验操作:把适量黑色固体置于试管中,加入适量的稀硫酸;实验现象:溶液变成黄色;实验结论:黑色固体是氧化铁.
③设铁的质量为x,
Fe+CuSO4═FeSO4+Cu,
56 64
X 6.4g
56:x=64:6.4g,x=5.6g,
则黑色固体B中铁单质的质量分数为:5.6g/7g×100%=80%.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案