题目内容
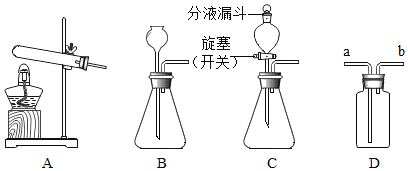
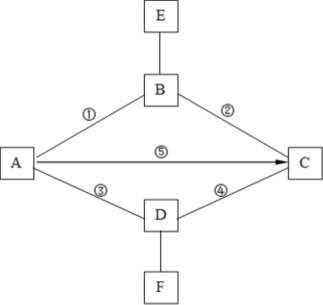
【题目】A、B、C、D、E是初中化学常见的物质,B是空气中含量第二位的物质,C是年产量最高的金属,D的浓溶液常作某些气体的干燥剂,其相互反应情况如图所示(“—”表示相连的物质能发生反应,“→”表示一种物质能生成另一种物质)。请回答:
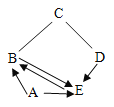
(1)写出A的化学式_______________________;
(2)简述把D的浓溶液变成稀溶液的方法_____________________________。
(3)C与D的稀溶液反应的化学方程式是____________________________。
【答案】H2O2 把浓硫酸沿着烧杯壁缓缓注入水中,并用玻璃棒不断搅拌 Fe + H2SO4 =FeSO4 + H2↑
【解析】
根据A、B、C、D、E是初中化学常见的物质,根据B是空气中含量第二位的物质,则B为氧气;根据C是年产量最高的金属,即C为铁;根据D的浓溶液常作某些气体的干燥剂,则D为硫酸;结合图框,则A为双氧水,E为水,代入检验,符合题意。
(1)根据分析,A为双氧水,A的化学式H2O2;
(2)根据分析,D为硫酸,故把硫酸的浓溶液变成稀溶液的方法:稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;切不可把水注入浓硫酸中。
(3)C与D的稀溶液反应,即铁与稀硫酸反应,反应的化学方程式是Fe+H2SO4═FeSO4+H2↑。
故答案为:
(1)H2O2;
(2)稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌。
(3)Fe+H2SO4═FeSO4+H2↑。

【题目】石灰石是常用的建筑材料。化学小组同学取一定量石灰石高温煅烧一段时间,冷却后,对剩余固体成分进行如下探究。
(1)写出石灰石高温煅烧的化学方程式___。
(2)根据化学方程式进行猜想。固体残留物成分:
I.只有氧化钙;II.只有碳酸钙;III.___
(3)甲乙丙三位同学分别设计了实验探究煅烧后固体成分。
友情提示:氯化钙溶液呈中性。
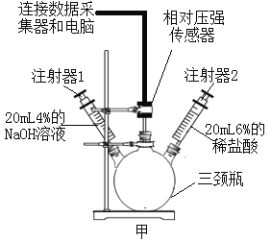
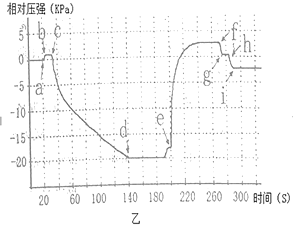
①甲同学取一定量的剩余固体于试管中,加入一定量的水振荡,用温度传感器测出溶液的温度,结果如图。则固体物质中一定含有___,用化学方程式解释判断的理由___。

②乙同学取一定量的剩余固体于试管中,加入足量的稀盐酸,待充分反应后,滴加酚酞试液,溶液呈无色。乙同学据此认为试管中的固体只有碳酸钙,即猜想 II成立。该同学设计方案是否合理,理由是___。
③丙同学利用水、无色酚酞溶液和稀盐酸证明了猜想III成立,请完成实验报告。
实验步骤 | 实验现象 | 实验结论 |
取少量剩余固体于试管中,加水振荡,过滤。 | 猜想III成立 | |
___ | ___ | |
___ | ___ |
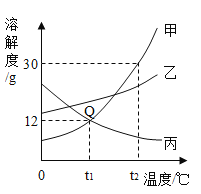
【题目】如图所示,在分别盛有100g水的烧杯中放入KNO3充分溶解,则说法正确的是( )
温度(℃) | t1 | t2 |
KNO3的溶解度(g/100g水) | 60 | 90 |
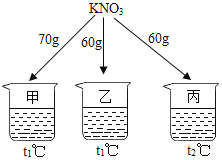
A. 甲、乙混合后为t1℃的不饱和溶液
B. 乙升温至t2℃,溶液质量增加
C. 乙、丙溶液中溶质质量相等
D. 丙降温至t1℃,有晶体析出