题目内容
【题目】碳酸钠在实际生产、生活中有着广泛的用途,如制造玻璃、造纸和纺织等。
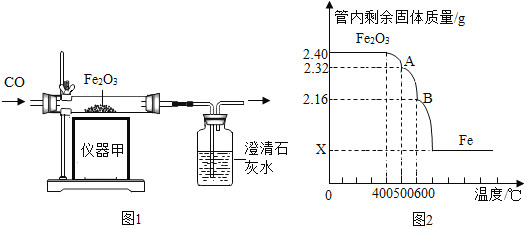
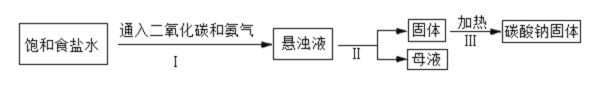
(1)碳酸钠俗称苏打或____。如图为侯氏制碱法的流程图,通过步骤I后得到的悬浊液中有小苏打(在该溶液中难溶)和一种氮肥,请写出步骤I中发生反应的化学方程式:_____;上述过程中得到的氮肥遇碱会生成具有刺激性气味的______(填化学式),该气体能使_____;从流程图中可得出小苏打的一条化学性质是_____。
(2)氢氧化钠在空气中容易变质生成碳酸钠,现有放在空气中一段时间的氢氧化钠溶液,其中溶质的成分可能是:猜想①:NaOH;猜想②:Na2CO3;猜想③:_____。请设计实验证明猜想③正确。(写出相关的步骤和现象)________
(3)某海洋化工集团生产的碳酸钠产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%。为测定该产品中碳酸钠的质量分数,现取11.0g碳酸钠样品放入烧杯中,称得烧杯及所盛碳酸钠样品的总质量为158.0g,然后向烧杯中加入100g稀盐酸,充分反应,实验数据记录如下:
反应时间/min | 3 | 6 | 9 | 12 |
烧杯及所盛物质的总质量/g | 255.8 | 254.0 | 253.6 | 253.6 |
请你据此分析计算,该产品中碳酸钠的质量分数_____(是、否)符合标准。(写出计算过程,结果精确到0.1%)
【答案】纯碱 NaCl+H2O+CO2+NH3=NaHCO3↓+NH4Cl NH3 湿润的红色石蕊试纸变蓝 受热易分解 NaOH和Na2CO3 取少量溶液于试管中,加入足量氯化钙溶液,出现白色沉淀,静置,取上层清液,向其中滴加无色酚酞溶液,溶液变红,猜想③正确 是
【解析】
(1)碳酸钠俗称苏打或纯碱;
由质量守恒定律可知,氯化钠、水、二氧化碳和氨气反应生成碳酸氢钠和氯化铵,反应的化学方程式为:NaCl+H2O+CO2+NH3=NaHCO3↓+NH4Cl;氯化铵遇碱会生成具有刺激性气味的氨气,化学式为:NH3;氨气易溶于水,形成氨水,氨水显碱性,故该气体能使湿润的红色石蕊试纸变蓝;由步骤Ⅲ可知,小苏打的一条化学性质是:受热易分解;
(2) 猜想①没有变质,为NaOH;猜想②全部变质,为Na2CO3;故猜想③为部分变质,为NaOH和Na2CO3;
取少量溶液于试管中,加入足量氯化钙溶液,出现白色沉淀,静置,取上层清液,向其中滴加无色酚酞溶液,溶液变红,猜想③正确;
(3)生成二氧化碳的质量=158.0g+100g-253.6g=4.4g
设样品中碳酸钠的质量为x。

![]()
x=10.6g
该产品中碳酸钠的质量分数=![]() ×100%=96.4%>96%
×100%=96.4%>96%
所以该产品符合标准。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案【题目】溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
(1)可以作为溶质的是__________。
A 只有固体 B 只有液体 C 只有气体 D 气体、液体、固体都可以
(2)在盛有水的烧杯中加入以下某种物质,形成溶液后,温度下降。这种物质可能是___。
A 氯化钠 B 硝酸铵 C 氢氧化钠 D 蔗糖
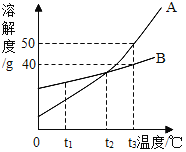
(3)下图为甲、乙、丙三种固体物质的溶解度曲线,请回答有关问题。
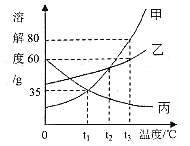
①将一瓶接近饱和的丙溶液变成饱和溶液,除通过增加溶质、蒸发溶剂使其达到饱和外,还可采取的方法__________。
②将t3℃时等质量的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液的质量由大到的顺序为___________。
③t3℃时,取甲、乙两物质配制溶液。
序号 | a | b | c | d | e |
固体种类 | 甲 | 甲 | 甲 | 乙 | 乙 |
甲固体的质量/g | 30 | 60 | 90 | 30 | 60 |
水的质量/g | 100 | 100 | 100 | 100 | 100 |
I.关于a~e所得溶液属于饱和溶液的是_________。
II.下列关于a~e所得溶液的说法不正确的是_____。
A b溶液恒温蒸发25g水后,与c溶液溶质质量分数相等
B e溶液的溶质质量分数为37.5%
C 将a、d溶液降温至t1℃,均有晶体析出
D c溶液恒温蒸发溶剂后,溶质质量分数变大