题目内容
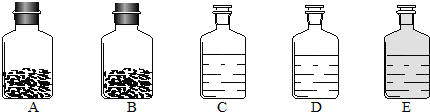
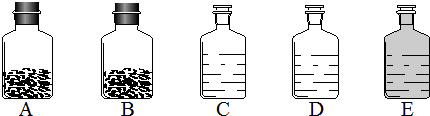
24、工业上的常说“三酸两碱”是重要的化工原料,也是重要的化工产品.如图是实验室桌面上的五个试剂瓶内分别装有属于工业上“三酸两碱”中的“三种浓酸”和“两碱固体”.

(1)小袁同学没有利用任何试剂就鉴定出了C、D、E三瓶中的三种浓酸.他的做法是:①直接观察试剂瓶颜色,棕色试剂瓶E内的是
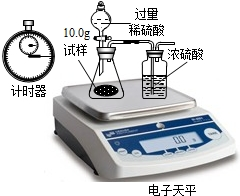
(2)小顾同学想利用D瓶内98%的浓硫酸来配制196g、10%的稀硫酸,他应取浓硫酸

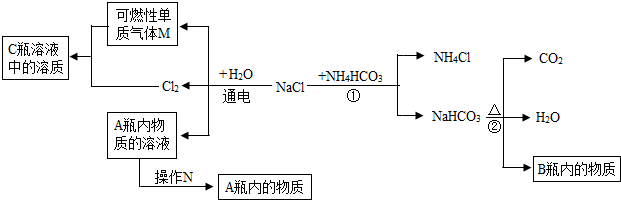
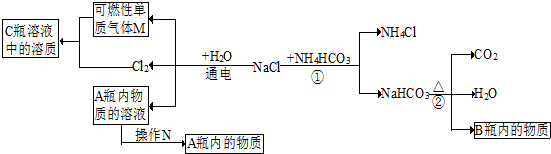
(3)小白同学在查阅A、B瓶内的“两碱”的制备方法时,根据收集的信息,绘制了如下一个框图.

注:整个框图中每个化学反应涉及的物质已全部给出.根据框图,回答下列问题.
[1]写出下列物质化学式:A瓶内的物质:
[2]框图中的①反应所属的反应类型是
[3]请写出物质转化的化学方程式A瓶内的物质→B瓶内的物质:

(1)小袁同学没有利用任何试剂就鉴定出了C、D、E三瓶中的三种浓酸.他的做法是:①直接观察试剂瓶颜色,棕色试剂瓶E内的是
浓硝酸
(填名称);②分别打开C、D瓶的瓶塞,看到C瓶的瓶口冒白雾,D瓶的瓶口无现象
,说明C瓶内的是浓盐酸
(填名称),D瓶内的是浓硫酸.(2)小顾同学想利用D瓶内98%的浓硫酸来配制196g、10%的稀硫酸,他应取浓硫酸
20
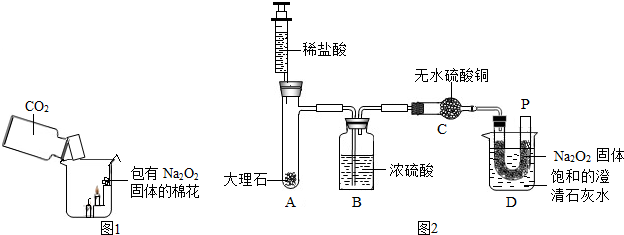
g.如图是小顾同学的配制方法,请指出他的两处错误:①将水倒入浓硫酸中
.②没有用玻璃棒搅拌
.
(3)小白同学在查阅A、B瓶内的“两碱”的制备方法时,根据收集的信息,绘制了如下一个框图.

注:整个框图中每个化学反应涉及的物质已全部给出.根据框图,回答下列问题.
[1]写出下列物质化学式:A瓶内的物质:
NaOH
;可燃性单质气体M:H2
.[2]框图中的①反应所属的反应类型是
复分解反应
;操作N是蒸发
.[3]请写出物质转化的化学方程式A瓶内的物质→B瓶内的物质:
2NaOH+CO2=Na2CO3+H2O
.分析:(1)根据酸的性质可知,浓硝酸见光易分解,则应保存在棕色试剂瓶,利用浓盐酸易挥发,而浓硫酸不挥发来区分.
(2)利用稀释前后硫酸的质量不变来计算,在稀释时应注意使产生的热量及时散失.
(3)根据框图中的反应和利用元素守恒的方法来确定物质及相关的问题.
(2)利用稀释前后硫酸的质量不变来计算,在稀释时应注意使产生的热量及时散失.
(3)根据框图中的反应和利用元素守恒的方法来确定物质及相关的问题.
解答:解:(1)因浓硝酸易见光分解,浓盐酸易挥发.
故答案为:浓硝酸;看到C瓶的瓶口冒白雾,D瓶的瓶口无现象(写冒白烟错误);浓盐酸.
(2)用98%的浓硫酸来配制196g、10%的稀硫酸,设浓硫酸的质量为X克,则X×98%=196×10%,解得X═20,稀释时应将密度大的倒入到密度小的液体中易混合均匀,并用玻璃棒搅拌及时散热.
故答案为:20;将水倒入浓硫酸中;没有用玻璃棒搅拌(写没有用玻璃棒、没有用玻璃棒引流错误).
(3)根据反应②知B为碳酸钠,C中是盐酸,则M为氢气,根据氯化钠和水通电发生的反应,则A为NaOH的溶液,将溶液蒸发可得到固体物质NaOH,则A中的物质为NaOH,反应①是化合物与化合物相互交换成分生成化合物与化合物,则属于复分解反应,A瓶内的物质→B瓶内的物质,可与二氧化碳或碳酸氢钠反应得到,
故答案为:[1]NaOH;H2
[2]复分解反应;蒸发
[3]2NaOH+CO2=Na2CO3+H2O(或NaOH+NaHCO3=Na2CO3+H2O)
故答案为:浓硝酸;看到C瓶的瓶口冒白雾,D瓶的瓶口无现象(写冒白烟错误);浓盐酸.
(2)用98%的浓硫酸来配制196g、10%的稀硫酸,设浓硫酸的质量为X克,则X×98%=196×10%,解得X═20,稀释时应将密度大的倒入到密度小的液体中易混合均匀,并用玻璃棒搅拌及时散热.
故答案为:20;将水倒入浓硫酸中;没有用玻璃棒搅拌(写没有用玻璃棒、没有用玻璃棒引流错误).
(3)根据反应②知B为碳酸钠,C中是盐酸,则M为氢气,根据氯化钠和水通电发生的反应,则A为NaOH的溶液,将溶液蒸发可得到固体物质NaOH,则A中的物质为NaOH,反应①是化合物与化合物相互交换成分生成化合物与化合物,则属于复分解反应,A瓶内的物质→B瓶内的物质,可与二氧化碳或碳酸氢钠反应得到,
故答案为:[1]NaOH;H2
[2]复分解反应;蒸发
[3]2NaOH+CO2=Na2CO3+H2O(或NaOH+NaHCO3=Na2CO3+H2O)
点评:本题考查知识点多,利用的方法是常用的方法,通过本题应掌握物质的区分和转化,能根据稀释过程来计算等.

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目