题目内容
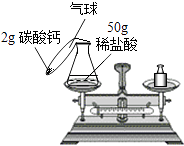
【题目】实验室常用加热氯酸钾与二氧化碳锰的混合物制取氧气,小军称取氯酸钾27g,加入0.2g二氧化锰进行加热.实验结束后,剩余固体残留物的质量为17.6g计算:
(1)反应后生成氧气的质量?
(2)生成氯化钾的质量为多少?
(3)氯酸钾是否完全分解?(请用计算说明)
【答案】
(1)解:生成氧气的质量为:27g+0.2g﹣17.6g=9.6g
(2)解:设生成氯化钾的质量为x,参加反应的氯酸钾质量为y
2KClO3 | 2KCl+ | 3O2↑ |
245 | 149 | 96 |
Y | X | 9.6g |
![]() =
= ![]() =
= ![]()
x=14.9g
y=24.5g
答:生成氯化钾的质量为14.9g。
(3)解:参加反应的氯酸钾质量为:24.5g<27g,所以氯酸钾没有完全分解
【解析】(1)根据质量守恒定律计算生成氧气的质量;(2)根据氧气的质量,依据化学方程式计算生成氯化钾的质量;(3)根据化学方程式计算参加反应的氯酸钾质量.
【考点精析】掌握根据化学反应方程式的计算是解答本题的根本,需要知道各物质间质量比=系数×相对分子质量之比.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
【题目】向装有某物质的烧杯中逐滴加入X溶液至过量,生成沉淀或气体的质量与加入X溶液的质量关系符合下图的是( )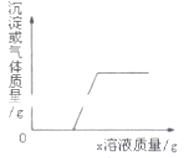
烧杯中的物质 | x溶液 | |
A | 稀H2SO4和CuSO4溶液 | NaOH溶液 |
B | 稀H2SO4和稀HCl | BaCl2溶液 |
C | Mg Al合金 | 稀HCl |
D | NaCl和NaHCO3 | 稀HCl |
A.A
B.B
C.C
D.D