题目内容
【题目】下图为实验室中常用装置。
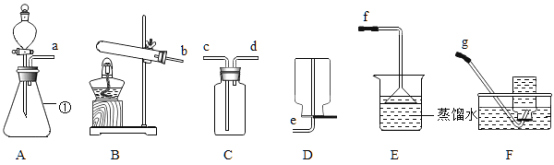
请回答下列问题:
(1)实验室用高锰酸钾制取并收集较纯净的氧气所选用的装置是__________(填装置字母),该反应的化学方程式为__________。二氧化锰直接排放会造成环境污染,从充分加热后的上述剩余固体中回收二氧化锰的方法是____________、过滤、洗涤和烘干(注:锰酸钾可溶于水)。
(2)夏天温度高,检查装置B的气密性,方法是:连接好仪器,把导管一端放入水中,然后______________,观察到有气泡冒出,说明装置气密性良好。
(3)实验室常用锌粒和稀硫酸制取氢气,其反应的化学方程式:____________。
(4)实验室制取二氧化碳的化学方程式是_____________,发生装置选取A的优点______________。
(5)通常状况下,氨气是一种无色、有强烈刺激性气味的污染性气体,极易溶解于水形成氨水,相同条件下密度比空气小。常温下实验室可以用浓氨水与生石灰制取氨气。请从上图中选出合适的仪器连接成一套制备并收集氨气的装置,则装置的接口连接顺序是a→_______→f,上述实验中,E装置的作用是____________。
【答案】BF ![]() 溶解 用热毛巾包裹试管或用酒精灯稍加热试管 Zn+H2SO4=ZnSO4+H2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ 能够控制反应速率 d→c 吸收多余的氨气,以防造成空气污染
溶解 用热毛巾包裹试管或用酒精灯稍加热试管 Zn+H2SO4=ZnSO4+H2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ 能够控制反应速率 d→c 吸收多余的氨气,以防造成空气污染
【解析】
(1)实验室用高锰酸钾制取氧气需要加热,应该用B装置作为发生装置;该反应的化学方程式:![]() ;因为氧气的密度比空气大,可以用向上排空气法收集,即用C装置收集,氧气不易溶于水,可以用排水法收集,即用F装置收集,用排水法收集的氧气比用排空气法收集的氧气纯净;从充分加热后的上述剩余固体中回收二氧化锰的方法是溶解、过滤、洗涤和烘干;
;因为氧气的密度比空气大,可以用向上排空气法收集,即用C装置收集,氧气不易溶于水,可以用排水法收集,即用F装置收集,用排水法收集的氧气比用排空气法收集的氧气纯净;从充分加热后的上述剩余固体中回收二氧化锰的方法是溶解、过滤、洗涤和烘干;
(2)检查装置B的气密性,方法是:连接好仪器,把导管一端放入水中,然后用热毛巾包裹试管或用酒精灯稍加热试管,观察到有气泡冒出,说明装置气密性良好;
(3)实验室常用锌粒和稀硫酸制取氢气,其反应的化学方程式:Zn+H2SO4=ZnSO4+H2↑;
(4)实验室制取二氧化碳的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑,发生装置选取A,A中使用分液漏斗,优点是:可以通过活塞控制液体的滴加速度进而控制反应速率;
(5)实验室中可以用浓氨水与生石灰制取氨气,属于固、液常温型,所以选择装置A来制取,氨气极易溶于水,密度比空气小,且污染空气,所以用装置C来收集(短进长出),最后装置E来吸收多余的氨气,以防造成空气污染,装置的接口连接顺序是a→d→c→f。

【题目】足球比赛中让意外昏迷的球员快速恢复意识会用到“嗅盐”。同学们对“嗅盐”产生了好奇,并对其成分进行了如下探究。
(查阅资料)
①嗅盐是一种盐类物质和香料(不参与下列探究中的任何反应)组成,能释放出氨味气体,对人体神经会产生强烈的刺激作用,但过量吸入会危害健康。
②氯化钙稀溶液与碳酸氢铵溶液不发生反应。
(提出问题)嗅盐中盐类物质是什么?
(实验探究)填写表中空格。
实验 | 小军的实验 | 小英的实验 | |
方案 |
嗅盐与___________(填一种物质)混合研磨 |
|
|
现象 | 闻到较浓烈刺激性气味且试纸变蓝 | ____________ | __________ |
结论 | 嗅盐中含有___________ | 嗅盐中含有CO32- | 确认了小军的实验结论 |
证明嗅盐中盐类物质是碳酸铵 | |||
(质疑)小英认为小军的实验不严谨,小英通过补做一个实验(方案见上表),进而确认了小军的结论。小英的实验目的是排除嗅盐中含有__________离子的可能性。
(继续探究)反应原理:(NH4)2CO3+2NaOH![]() X+2NH3↑+2H2O,其中X的化学式为________。
X+2NH3↑+2H2O,其中X的化学式为________。