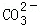题目内容
某化学兴趣小组的同学往氢氧化钠溶液中滴加稀盐酸时,没有看到明显现象.
【提出问题】氢氧化钠与盐酸是否发生了化学反应?
【查阅资料】酸与碱发生中和反应会放出热量.
【实验设计】甲、乙、丙三位同学分别设计了如下实验方案,请你帮他们完成实验报告.
【评价反思】你认为实验设计方案不合理的同学是 ,理由是 .
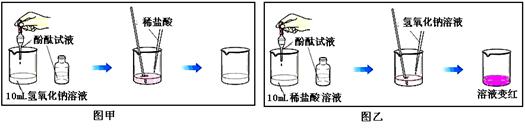
【拓展延伸】另有一位同学向自己配制的氢氧化钠溶液中滴加酚酞试液时,溶液变红色,可是红色即可消失了,出现此意外情况的原因是 (填以下序号).
A.所用的酚酞试液是变质的
B.所用的氢氧化钠溶液浓度太小
C.氢氧化钠溶液吸收了空气中二氧化碳
【提出问题】氢氧化钠与盐酸是否发生了化学反应?
【查阅资料】酸与碱发生中和反应会放出热量.
【实验设计】甲、乙、丙三位同学分别设计了如下实验方案,请你帮他们完成实验报告.
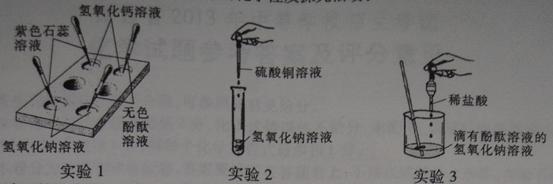
| 同学 | 实验操作 | 现象 | 结论 |
| 甲 | 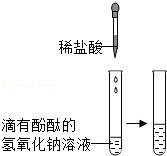 | 溶液由红色变成 | 氢氧化钠与盐酸发生了化学反应,反应的化学方程式为 |
| 乙 |  | U型玻璃管中 边的红墨水液面下降(所加稀盐酸的体积忽略不计) | 氢氧化钠与盐酸发生了化学反应 |
| 丙 | 用 测定氢氧化钠溶液的pH,向其中滴加足量稀盐酸,再测定溶液的pH | 最后溶液的pH (填“≥7”、“≤7”、“不变” | 氢氧化钠与盐酸发生了化学反应 |
【评价反思】你认为实验设计方案不合理的同学是 ,理由是 .
【拓展延伸】另有一位同学向自己配制的氢氧化钠溶液中滴加酚酞试液时,溶液变红色,可是红色即可消失了,出现此意外情况的原因是 (填以下序号).
A.所用的酚酞试液是变质的
B.所用的氢氧化钠溶液浓度太小
C.氢氧化钠溶液吸收了空气中二氧化碳
[实验设计]甲:无色;HCl+NaOH=NaCl+H2O;乙:左;丙:pH试纸;≤7;[评价反思]乙;氢氧化钠固体溶于水也会放出热量;[拓展延伸]B.
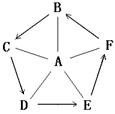
试题分析:【实验设计】酚酞试液遇到碱溶液变红,遇到中性溶液或酸性溶液不变色,所以氢氧化钠中滴加盐酸使,当把氢氧化钠反应完了,溶液就会变为无色;反应物是氢氧化钠和盐酸,生成物是氯化钠和水,所以方程式是:HCl+NaOH=NaCl+H2O;
氢氧化钠固体溶于水会放出大量的热,氢氧化钠与盐酸反应也能放出热量,会导致瓶内温度升高,由于热胀冷缩,所以U型玻璃管中液面左侧下降右侧上升;
测定溶液的pH最简单的方法是使用pH试纸;中性溶液或酸性溶液都不能使酚酞试液变色所以最后所得溶液的pH值可能小于7,也可能等于7;
【评价反思】由于氢氧化钠固体溶于水会放出热量,到底热量是氢氧化钠与盐酸反应放出的,还是氢氧化钠固体溶于水放出的,无法判断,所以乙同学的实验现象不能说明氢氧化钠与盐酸发生了反应;
【拓展延伸】由于溶液变红色了,说明酚酞试液没有变质,故A错;氢氧化钠溶液吸收了空气中二氧化碳生成碳酸钠,也是显碱性,也能使酚酞试液变红,所以C答案错误;如果氢氧化钠溶液浓度太小会造成,开始滴加酚酞变红,红色即可消失.故选B.
点评:本题是已设计的实验方案进行评价,以及自己设计实验方案的题目,要注意考虑所涉及物质的化学性质,据它们的化学性质来设计方案,这是我们解题的大方向.

练习册系列答案
相关题目