题目内容
某天化学兴趣小组听老师讲:“浓硫酸加衣服等于洞洞眼眼,还有刺激性气味产生”.兴趣小组结合浓硫酸的性质思考,难道浓硫酸能与碳单质反应?若反应,会生成什么呢?
[查阅资料]:
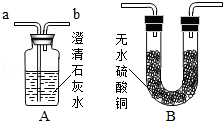
①SO2能使澄清石灰水变浑浊 Ca(OH)2+SO2=CaSO3+H2O;
②SO2能使品红溶液褪色,用于检验SO2存在;
③SO2能与溴水反应而被吸收 SO2+Br2+2H2O=H2SO4+2HBr.
[提出猜想]:从物质组成元素看,可能生成H2、CO2、CO、SO2气体及H2O;
[实验步骤]:实验小组设计了如下步骤:
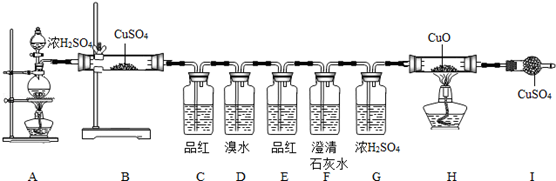
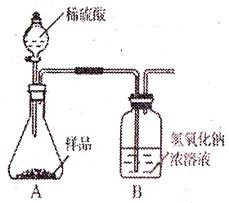
(1)按上述图示安装好仪器;
(2)检查气密性;
(3)加入对应药品,并将浓H2SO4放入烧杯中;
(4)加热A,加热H;
(5)停止加热.
[实验分析]:
(1)B处,固体由白色变蓝色,说明有H2O生成;
(2)C处,品红溶液褪色,说明有 (填化学式)生成;
(3)E处,品红溶液不褪色,说明 (填化学式)已被除尽;
(4)F处,澄清石灰水变浑浊,则产生浑浊的化学方程式为 ;
(5)H、I处无现象,说明无CO、H2生成.
[实验结论]:
(1)气体中有H2O和 生成,无CO、H2生成;
(2)浓硫酸能与碳单质反应,其化学方程式为 .
[查阅资料]:
①SO2能使澄清石灰水变浑浊 Ca(OH)2+SO2=CaSO3+H2O;
②SO2能使品红溶液褪色,用于检验SO2存在;
③SO2能与溴水反应而被吸收 SO2+Br2+2H2O=H2SO4+2HBr.
[提出猜想]:从物质组成元素看,可能生成H2、CO2、CO、SO2气体及H2O;
[实验步骤]:实验小组设计了如下步骤:

(1)按上述图示安装好仪器;
(2)检查气密性;
(3)加入对应药品,并将浓H2SO4放入烧杯中;
(4)加热A,加热H;
(5)停止加热.
[实验分析]:
(1)B处,固体由白色变蓝色,说明有H2O生成;
(2)C处,品红溶液褪色,说明有 (填化学式)生成;
(3)E处,品红溶液不褪色,说明 (填化学式)已被除尽;
(4)F处,澄清石灰水变浑浊,则产生浑浊的化学方程式为 ;
(5)H、I处无现象,说明无CO、H2生成.
[实验结论]:
(1)气体中有H2O和 生成,无CO、H2生成;
(2)浓硫酸能与碳单质反应,其化学方程式为 .
[实验分析](2)SO2; (3)SO2; (4)Ca(OH)2+CO2=CaCO3↓+H2O;
[实验结论](1)SO2 CO2;(2)C+2H2SO4(浓)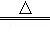 CO2↑+2SO2↑+2H2O.
CO2↑+2SO2↑+2H2O.
[实验结论](1)SO2 CO2;(2)C+2H2SO4(浓)
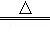 CO2↑+2SO2↑+2H2O.
CO2↑+2SO2↑+2H2O.试题分析:[实验分析]:(2)因为SO2能使品红溶液褪色,所以C处品红溶液褪色,说明有二氧化硫生成;
(3)因为SO2能在D装置中与溴水反应而被吸收,所以E处,品红溶液不褪色,说明二氧化硫已经被除尽;
(4)因为二氧化硫已经被除尽,而F处澄清石灰水变浑浊,说明有二氧化碳气体的产生,发生反应的方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
[实验结论](1)综合分析实验现象可以看出产生的气体有H2O和SO2 CO2,无CO、H2生成.
(2)因此浓硫酸和碳反应的方程式为:C+2H2SO4(浓)
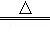 CO2↑+2SO2↑+2H2O.
CO2↑+2SO2↑+2H2O.点评:本题属于信息题的考查,难度不大,结合题目提供的有效信息结合已有的相关知识逐步分析即可解决问题.

练习册系列答案
相关题目
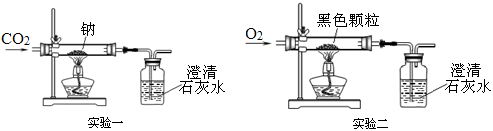
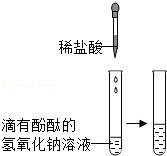

 ① ;
① ;