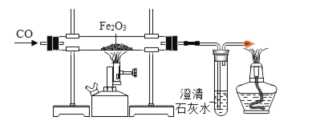
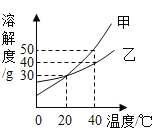
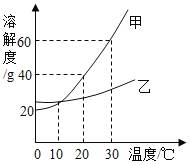
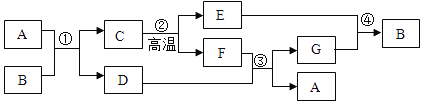
题目内容
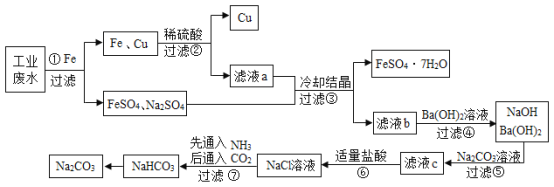
【题目】某活动小组用废铜制取硫酸铜溶液,实验过程为:
![]()
⑴ 废铜在空气中加热后得到的氧化铜中含有少量铜,原因是 _________(填字母序号)。
a.加热时氧化铜易分解生成铜
b.铜与氧气没有完全反应
c.加热时铜不能与氧气反应
⑵ 氧化铜与稀硫酸反应的化学方程式为 。
⑶ 操作Ⅰ的名称是________,该操作用到的玻璃仪器有:玻璃棒、烧杯、 。
⑷ 盛放硫酸铜溶液不宜用铁制容器的原因是(用化学方程式解释) 。
【答案】(1) b (2)CuO+H2SO4=CuSO4+H2O
(3)过滤、漏斗 (4)Fe+CuSO4=FeSO4+Cu
【解析】
试题(1)铜在空气中加热时,生成的氧化铜会覆盖在铜的表面,使里面的铜不能和氧气接触,不能完全反应,故选b;
(2)氧化铜与稀硫酸反应生成硫酸铜和水,故反应的化学方程式为 CuO+H2SO4=CuSO4+H2O;
(3)过滤是分离固体(铜)与液体(硫酸铜溶液)混合物的一种方法,故操作Ⅰ的名称是过滤,该操作用到玻璃仪器有,烧杯、玻璃棒和漏斗;
(4)因为铁比铜活泼,故铁能与硫酸铜溶液反应生成铜和硫酸亚铁,故反应的化学方程式为Fe+CuSO4═FeSO4+Cu。

【题目】某化学研究性学习小组在实验室进行了化学实验,向一盛有锌和铜混合物的烧杯中加入一定量的稀硫酸,充分反应后,观察到烧杯中有固体剩余,对反应后所得溶液中溶质的成分进行探究。
(1)写出上述烧杯中发生反应的化学方程式______。
(2)对反应后所得溶液中溶质的成分进行猜想,请你再补充一种猜想。
(猜想)猜想一:溶质为硫酸锌;
猜想二:溶质为硫酸铜和硫酸锌;
猜想三:溶质为______。
(3)(讨论)你认为猜想______不合理,理由是______。
(4)(实验)若猜想三正确,完成下列实验方案证明你的猜想。
实验步骤 |
| 实验结论 |
用玻璃棒蘸取少量待测液滴到 | _______ | 猜想三正确 |
(5)(应用)如果猜想三正确,把该废液倒入铁质下水管道可能造成危害,为消除此废液可能带来的危害,一般会在废液中加入适量的熟石灰,请写出此反应的化学方程式:_______。