题目内容
【题目】【2014年四川省达州市】今年化学实验操作考试中,有一题目是鉴别澄清石灰水和氢氧化钠溶液。请你参与探究:
[提出问题]如何鉴别这两种无色溶液?
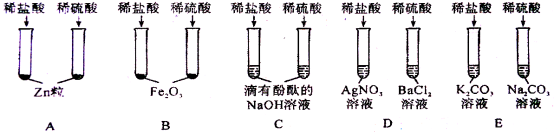
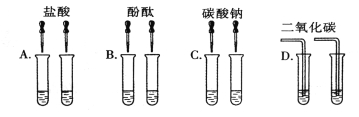
[实验方案]小琪等几位同学进行了下图所示的实验。
请你回答下列问题:
(1)C组实验中反应的化学方程式为 ;
(2)其中不能达到实验目的的是 (填字母);
(3)D组实验中变浑浊的原溶液是 。
[继续探究]实验结束后,小琪同学将A、B、C、D四组试管中的物质全部倒入同一个干净的烧杯中,充分反应后,得到无色澄清透明的溶液,对该溶液的成分又进行了探究。
[提出问题]该溶液中除水、酚酞外还含有哪些物质?
[查阅资料]氯化钙溶液呈中性。
[猜想与假设]Ⅰ.
Ⅱ.NaCl、CaCl2、HCl
Ⅲ.NaCl、CaCl2、NaOH
[反思与拓展]①上述猜想与假设中只有一个不成立,它是 (填序号),理由是 。
②根据所学化学知识,验证烧杯内溶液中可能有的物质是否存在,下列哪些物质单独使用不能完成该实验
(填字母)
a.pH试纸
b.硝酸银溶液
c.紫色石蕊试液
d.铜
e.足量氢氧化钠溶液
【答案】【实验方案】(1)Na2CO3 +Ca(OH)2==CaCO3↓+ 2NaOH;
(2)A、B;
(3)澄清石灰水或Ca(OH)2溶液;
【猜想与假设】ⅠNaCl、 CaCl2;
【反思与拓展】①Ⅲ;NaOH溶液能使无色酚酞试液变红,不能得到无色溶液(合理答案均给分);②b、d
【解析】
试题分析:氢氧化钠和氢氧化钙都属于碱,只是金属阳离子不同,可用来鉴别;(1)碳酸钠与氢氧化钠不反应,与氢氧化钙反应生成白色沉淀:Na2CO3 +Ca(OH)2==CaCO3↓+ 2NaOH;(2)产生不同现象才能鉴别,A组盐酸与两种物质反应均无明显现象,不能鉴别;(3)二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀,故D组实验中变浑浊的原溶液是氢氧化钙溶液;[猜想与假设]中 Ⅱ.NaCl、CaCl2、HCl Ⅲ.NaCl、CaCl2、NaOH中氯化氢和氢氧化钠为反应剩余物,NaCl、CaCl2为反应生成物,一定含有,故Ⅰ.为NaCl、CaCl2;[反思与拓展]①因为实验中用到酚酞,若含有氢氧化钠应显红色,与实验现象不符,故猜想Ⅲ不成立;②要验证烧杯内溶液中可能有的物质(即盐酸)是否存在,应依据题意及盐酸的化学性质进行设计,硝酸银与氯化钠、氯化钙及盐酸均能产生白色沉淀,无法证明盐酸说法存在;铜与盐酸不反应,不能验证盐酸的存在;故选b、d 。

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案