题目内容
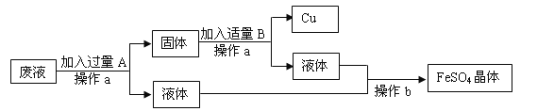
【题目】某同学收集了班级同学做完“氢气还原氧化铜”实验后的固体残渣(含铜和氧化铜),欲从中回收单质铜和制取硫酸铜溶液,他设计了如下实验方案:
(1)称量。称量收集到的固体残渣20g,需要的仪器名称是_____。
(2)溶解。将20g称量好的固体残渣放入烧杯中,加入过量的稀硫酸溶液,用玻璃棒不断搅拌,直至反应完全。烧杯中发生反应的化学方程式是_____。
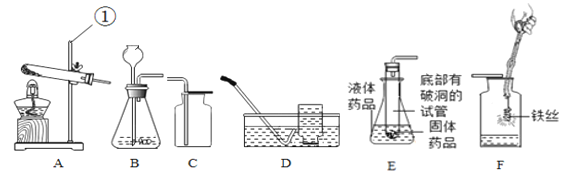
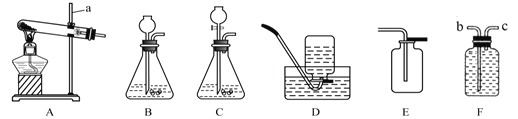
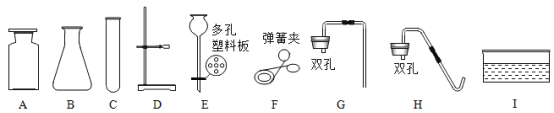
(3)过滤。除滤纸外,还需要从下图中选用的仪器是______(填字母)。
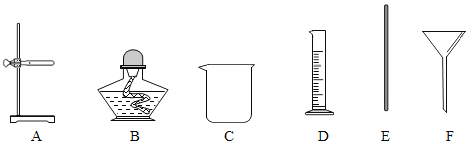
(4)洗涤干燥。洗净滤纸上的固体,干燥后称量,此固体名称为_______。
(5)收集滤液。滤液中所含溶质的化学式是_____。
(6)分析。为了进一步达到实验目的,应往滤液中加入过量的下列_____(填编号)固体粉末,过滤。①氧化铜;②氢氧化钠;③铁;④硫酸铜。在滤液中加入过量的固体粉末,原因是______,实验现象是______。
【答案】天平 CuO+H2SO4=CuSO4+H2O ACEF 铜 CuSO4、H2SO4 ① 除去过量硫酸 仍有部分固体剩余
【解析】
(1)称量收集到的固体残渣20g,需要的仪器名称是托盘天平;
(2)将20g称量好的固体残渣放入烧杯中,加入过量的稀硫酸溶液,用玻璃棒不断搅拌,直至反应完全。铜与稀硫酸不反应,氧化铜与稀硫酸反应原理CuO+H2SO4=CuSO4+H2O;
(3)除滤纸外,还需要从下图中选用的仪器是:A铁架台,用于固定仪器、C烧杯,用于承接滤液、E玻璃棒,用于引流、F漏斗,用于过滤;
(4)洗净滤纸上的固体,干燥后称量,此固体只有铜为溶解,固体名称为:铜;
(5)滤液中所含溶质的化学式是:CuSO4、 H2SO4的混合溶液;
(6)为了进一步达到实验目的,应往滤液中加入过量的①氧化铜固体粉末,过滤。在滤液中加入过量的氧化铜固体粉末,原因是除去过量硫酸,实验现象是:仍有部分固体剩余。