题目内容
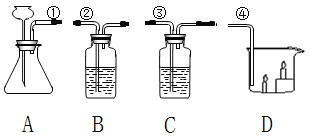
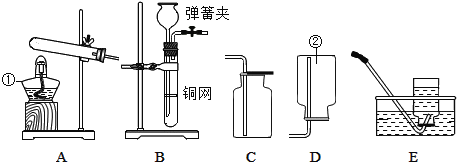
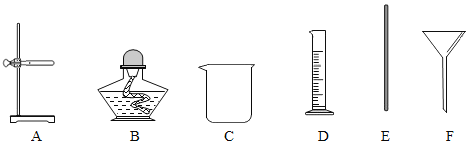
【题目】下图是实验室常用的实验装置,请回答下列问题。
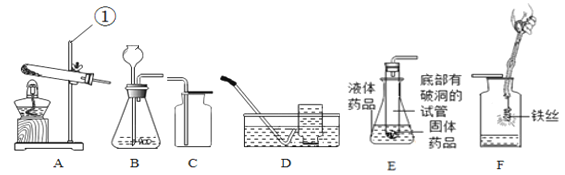
(1)写出仪器①的名称_____。
(2)用高锰酸钾制取氧气,选用的发生装置是_____(填序号),反应的化学方程式为_____,若用D装置收集氧气,当观察到气泡_____冒出时,便可开始收集。
(3)实验室制取二氧化碳应选用的一组装置是_____(填序号),反应的化学方程式是_____。图E是某同学利用报废试管设计的制二氧化碳的发生装置,该设计除了废物利用的优点外,请另写一个优点:_____。
(4)用收集的氧气完成图F铁丝燃烧的实验,反应的化学方程式为_____。
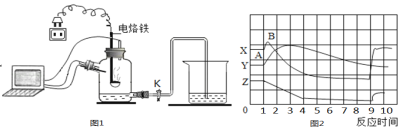
(5)某化学兴趣小组在老师指导下制取、干燥、收集氨气,并探究氨气的一些性质.
(查阅资料)
a.氨气通常情况下是有刺激性气味的无色气体,密度比空气小,极易溶于水.
b.氨水是氨气(NH3)的水溶液,具有碱的性质。
c.碱能使无色酚酞溶液变红。
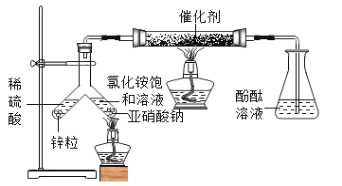
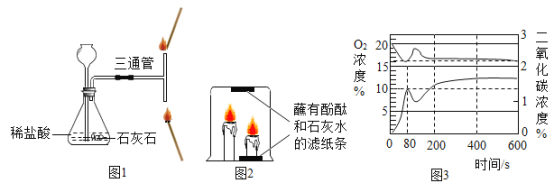
图为合成氨的模拟实验装置图(玻璃管中是铁粉和石棉绒组成的混合物)。
步骤:①检查气密性;②使锌粒和稀硫酸反应一段时间;③在Y型管盛有亚硝酸钠和氯化铵饱和溶液的一边加热(NH4Cl + NaNO2![]() NaCl + 2H2O + N2↑ );④到产生氮气较快时,再点燃玻璃管下方的酒精灯进行加热。
NaCl + 2H2O + N2↑ );④到产生氮气较快时,再点燃玻璃管下方的酒精灯进行加热。
①反应开始前使锌粒和稀硫酸反应一段时间的目的是:_____。
②当锥形瓶中出现_____现象,表示有氨气生成。
③写出玻璃管中生成氨气的化学方程式_____。
【答案】铁架台 A ![]() 连续均匀 BC CaCO3+2HCl═CaCl2+H2O+CO2↑ 可以控制反应发生与停止
连续均匀 BC CaCO3+2HCl═CaCl2+H2O+CO2↑ 可以控制反应发生与停止 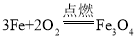 排尽装置内的空气,防止爆炸;同时提高氢气浓度从而提高氮气转化率 酚酞溶液变红
排尽装置内的空气,防止爆炸;同时提高氢气浓度从而提高氮气转化率 酚酞溶液变红 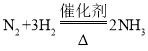
【解析】
(1)仪器①的名称是:铁架台;
(2)用高锰酸钾制取氧气时,需要加热,故选发生装置A;高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式为:![]() ;若用D装置收集氧气,当观察到气泡连续均匀冒出时,便可开始收集。
;若用D装置收集氧气,当观察到气泡连续均匀冒出时,便可开始收集。
(3)实验室制取二氧化碳是用碳酸钙和稀盐酸反应制取的,根据反应物状态、反应条件选择发生装置是B,二氧化碳密度比空气大,可以用向上排空气法收集,收集装置选择C;碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;图E另一个优点是可以控制反应发生与停止;
(4)用收集的氧气完成图F铁丝燃烧的实验,铁丝在纯氧中点燃生成四氧化三铁,反应的化学方程式为: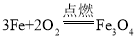 ;
;
(5)①反应开始前使锌粒和稀硫酸反应一段时间的目的是排出装置内部的空气,防止可能发生的爆炸,同时生成尽可能多的氢气,提高氢气浓度从而提高氮气的转化率。
②氨气溶于水显碱性,酚酞溶液遇碱变红,所以当锥形瓶中出现酚酞溶液变红现象,表示有氨气生成;
③根据题意分析,玻璃管中生成氨气的化学方程式为: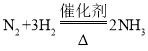 。
。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案【题目】(第一组实验)在试管中加入5mL久置的“双氧水”,把带火星的木条伸入试管中,发现木条未复燃:②用酒精灯给上述试管加热,液体中有气泡产生,把带火星的木条伸入试管中,发现木条仍未复燃;③如图装置进行操作,带火星的木条复燃,
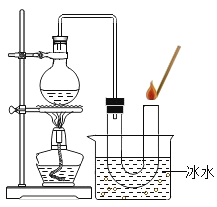
(1)烧杯中冰水所起的作用是_____________________。
(2)②中木条未复燃的原因是 _________________________。
(第二组实验)Mg(OH)2是一种新型的阻燃剂,某同学用氨水在实验室模拟制取Mg(OH)2 的过程:在一定温度下,往一定量的氯化镁中加入氨水(氨水易挥发),生成Mg(OH)2,再通过结晶、过滤,得到Mg(OH)2晶体。为探究获得较高Mg(OH)2晶体转化率的条件,该同学进行下述对比实验,数据如下:
实验编号 | 氯化镁溶液浓度/g/L | 反应温度/℃ | Mg(OH)2转化率/% |
a | 20 | 30 | 27.06 |
b | 40 | 30 | 56.77 |
c | 40 | 40 | 69.64 |
d | 40 | 60 | 54.30 |
e | 60 | 60 | 50.60 |
①实验b和c的目的是________________。
②在氯化镁溶液浓度是40g/L的情况下,60℃时Mg(OH)2的转化率比40℃时低的原因是________________。
③由实验数据可知,能够得到最多Mg(OH)2的条件是______g/L和_________ ℃
④为了提升设备利用效率和节约能源,可进一步优化反应条件,若再设计对比实验,选择的实验条件(氯化镁溶液浓度和温度)还可以是____________(填选项)
A 60,70℃ B 45,45℃ C 38,40℃ D 40,35℃