题目内容
【题目】化石燃料在当今社会能源中担当“主角”。
(1)化石燃料包括煤、______和天然气。
(2)天然气是生活中常用的燃料,其主要成分充分燃烧的化学方程式是________。
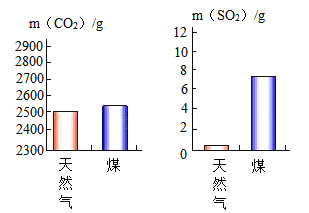
(3)分别充分燃烧1000 g天然气、煤所产生的CO2和SO2气体的质量如下图所示,根据图示分析,则________燃烧产生的气体更易导致酸雨。
(4)洁净的空气对人类非常重要。下列做法不利于保护大气的是________(填序号)
A燃煤取暖改为天然气供暖 B积极植树造林
C工业废气净化后排放 D焚烧落叶和垃圾
(5)为减少污染、提高煤的利用率,也可将煤与水蒸气在高温下反应转化为两种常见的可燃性气体,该反应的化学方程式为_________。
(6)化石燃料的广泛使用不仅造成酸雨,还能导致______,致使全球变暖,极端天气多发。为减缓全球变暖,应大力开发下列哪些能源______。
A石油 B地热能 C太阳能 D氢能
【答案】石油 CH4+2O2![]() CO2+2H2O 煤 D C+H2O
CO2+2H2O 煤 D C+H2O![]() CO+H2 温室效应 BCD
CO+H2 温室效应 BCD
【解析】
(1)化石燃料包括煤、石油和天然气。
(2)天然气主要成分是甲烷,充分燃烧时生成二氧化碳和水,化学方程式是CH4+2O2![]() CO2+2H2O。
CO2+2H2O。
(3)导致酸雨形成的气体是SO2气体,根据图示分析,煤燃烧产生的二氧化硫远远大于甲烷燃烧产生的二氧化硫,则煤燃烧产生的气体更易导致酸雨。
(4)A、燃煤取暖改为天然气供暖,减少二氧化硫的排放,减少酸雨的形成,不符合题意;
B、积极植树造林,减少空气中的二氧化碳,减少温室效应的加剧,不符合题意;
C、工业废气净化后排放,减少有害气体的排放,不符合题意;
D、焚烧落叶和垃圾,产生有害气体和烟尘,污染环境,符合题意。故选 D。
(5)将煤与水蒸气在高温下反应转化为两种常见的可燃性气体,煤的主要成分是碳,水中有氢、氧元素,所以该反应生成的两种常见可燃性气体为氢气和一氧化碳,反应的化学方程式为C+H2O![]() CO+H2。
CO+H2。
(6)化石燃料的燃烧生成二氧化碳、二氧化硫、二氧化氮等,不仅造成酸雨,还能导致温室效应,致使全球变暖,极端天气多发。为减缓全球变暖,应大力开发地热能、太阳能、氢能等新能源。

 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案【题目】下列化学方程式及其反应类型都正确的是( )
选项 | 化学方程式 | 反应类型 |
A | Mg+O2 | 化合反应 |
B | H2O2 | 分解反应 |
C | Fe+H2SO4=FeSO4+H2↑ | 置换反应 |
D | 2KNO3+Ba(OH)2=Ba(NO3)2+2KOH | 复分解反应 |
A.AB.BC.CD.D
【题目】在研究酸和碱的化学性质时,同学们想证明:稀H2SO4与NaOH溶液确实发生了反应。请你与他们一起完成实验方案设计、实施和评价。(注:硫酸钠溶液呈中性)
(1)向NaOH溶液中滴入2~3滴酚酞溶液,溶液由无色变为__________色。
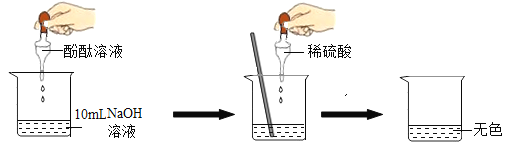
(2)根据上述实验中颜色变化,确定稀H2SO4与NaOH溶液发生了化学反应,反应的化学方程式为____________。
(3)因为溶液变成了无色,小林说“稀硫酸一定过量了”,小林这么说的理由是_____________。
(4)为确定小林的说法是否正确,同学们又设计了下列实验方案并进行实验:
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀H2SO4过量 |
方案二一 | 取样,滴入2-3滴紫色石蕊溶液 | 溶液变成红色 | 稀H2SO4过量 |
上述方案中,你认为正确的是____________(填“方案一”或“方案二”)。另外一个实验方案错误的原因(用化学方程式表示): ______________。请你再设计一种实验方案确定稀H2SO4过量,你选用___________(填药品)。