题目内容
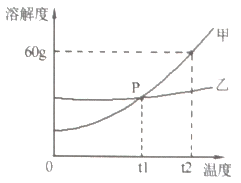
【题目】如图是初中化学中常见物质间的转化关系,其中甲、乙为单质,A、B、C、D为化合物,且A与B的组成元素相同,C与D的组成元素也相同。其余反应条件、部分反应物已略去。试推断:

![]() 写出有关物质的化学式:
写出有关物质的化学式:
A:______;乙:______;C:______。
![]() 写出下列化学方程式:
写出下列化学方程式:
![]() 甲:______;
甲:______;
![]() :______。
:______。
【答案】![]()
![]() CO 2H2O2
CO 2H2O2![]() 2H2O+ O2↑ 2CO+O2
2H2O+ O2↑ 2CO+O2![]() 2CO2(合理即可)
2CO2(合理即可)
【解析】
A与B的组成元素相同,A能转化为B和甲,过氧化氢在二氧化锰催化作用下分解生成水和氧气,所以可猜想A是过氧化氢,B和甲是水和氧气中的一种,B能够分解生成甲和乙,水通电分解生成氧气和氢气,所以甲是氧气,乙是氢气;C与D的组成元素相同,甲(氧气)能转化为D,甲(氧气)能转化为C,C能转化为D,碳在氧气中充分燃烧生成二氧化碳,碳在氧气中不完全燃烧生成一氧化碳,一氧化碳在氧气中燃烧生成二氧化碳,所以C可以是一氧化碳,D可以是二氧化碳,代入原框图,推断合理。
根据以上分析可知:
(1)由分析知A是过氧化氢,化学式为:![]() ;乙是氢气,化学式为:
;乙是氢气,化学式为:![]() ;C是一氧化碳,化学式为:CO;
;C是一氧化碳,化学式为:CO;
(2)A→B+甲是过氧化氢在二氧化锰催化作用下分解生成水和氧气的反应,化学方程式为:2H2O2![]() 2H2O+ O2↑,
2H2O+ O2↑,![]() 可以由一氧化碳与氧气反应完成,化学方程式为:2CO+O2
可以由一氧化碳与氧气反应完成,化学方程式为:2CO+O2![]() 2CO2。
2CO2。

【题目】某兴趣小组在实验室里准备常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中,有一瓶未盖瓶塞且标签破损的溶液(如图),他们决定对这瓶溶液的成分进行探究。

(提出问题)这瓶溶液的溶质是什么?
(获得信息)
①酸、碱、盐的性质实验中用到含钠元素的物质有氯化钠、氢氧化钠、碳酸钠、碳酸氢钠。
②实验室里盛放碱性溶液的试剂瓶通常使用橡胶塞。
③氯化钡溶液呈中性。
(提出猜想)猜想一:氢氧化钠:猜想二:碳酸钠:猜想三:碳酸氢钠。
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
取一支洁净试管,加入待测液,然后滴加过量稀盐酸 | 有 ______ 产生 | 该溶液的溶质是碳酸钠或者是 ______ |
再取一支洁净试管,加入待测液,后加入过量的氯化钡溶液 | 有白色沉淀产生 | 该溶液的溶质是 ______ ,发生 反应的化学方程式为 ______ |
小华认为上面的结论不完全正确,理由是______(用化学方程式表示);小组讨论后,又进行如下实验:
取第二次实验后的上层清液,滴入无色酚酞试液,溶液呈红色。
(实验结论)这瓶溶液的原溶质是氢氧化钠。
(交流反思)实验探究中,能否用氢氧化钡溶液替代氯化钡溶液?______(填“能”或“不能”):实验中取用液体药品时,应注意密封保存。