题目内容
【题目】在有催化剂存在并加热的条件下,A(氨气)与B反应生成C(一氧化氮)和D.反应前后分子变化的微观示意图如图所示,下列说法正确的是( )
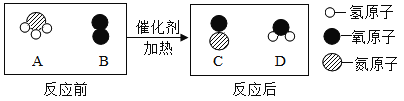
A. 该反应的基本反应类型为分解反应
B. 上述四种物质中有两种属于氧化物
C. 反应前后元素的化合价均不变
D. 生成物中两种物质的质量比为5:3
【答案】B
【解析】
由反应前后分子变化的微观示意图可知,该反应是氨气和氧气在在催化剂并加热的条件下反应生成了一氧化氮和水,反应的方程式是:4NH3+5O2![]() 4NO+6H2O。
4NO+6H2O。
A、该反应的反应物是两种,不属于分解反应,故A错误;
B、4种物质中C、D分别是一氧化氮和水,都属于氧化物,故B正确;
C、有单质氧气参加反应,反应前后,氧元素的化合价一定改变,故C错误;
D、由方程式可知,生成物中两种物质的质量比为:(30×4):(18×6)=10:9,故D错误。
故选B。

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
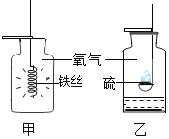
小学课时特训系列答案【题目】化学兴趣小组探究金属的性质时,将一段去除氧化膜的镁条,放入一定量的稀盐酸中,有气泡产生,充分反应后静置,发现试管中有灰白色沉淀。写出产生气泡的反应化学方程式______。
(提出问题)灰白色沉淀是什么物质?
(猜想假设)①小华认为灰白色沉淀为碳酸镁(MgCO3),其他同学认为不需要实验就能否定小华的猜想,理由是_____________________。
②小宇认为由于反应后氯化镁的生成量偏多,灰白色沉淀为不能再溶解的氯化镁固体。
③小彤认为灰白色沉淀为__________________。
(实验探究1)
实验操作 | 现象 | 结论 |
①取试管中的上层清液,加入适量的氯化镁固体 | 氯化镁固体__(选填“溶解”或“不溶解”) | 小宇猜想错误 |
②取适量白色沉淀加入足量稀盐酸中 | 没有气泡冒出 | 小彤猜想错误 |
基于以上探究与分析,原有猜想均遭到了否定。
(查阅资料)
HCl+AgNO3═HNO3+AgCl↓,AgCl是一种白色沉淀。氯化氢是酸性气体,能使蓝色石蕊试纸变红。进行
(实验探究2)
他们又另取灰白色沉淀放入试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管内,玻璃棒上的溶液出现白色浑浊,证明产生了__气体。如何检验这种气体_______(实验步骤、现象、结论)。
同学们请教老师后得知,足量的镁与稀盐酸反应时,溶液会经历从酸性到碱性且碱性逐步增强的过程,从而生成了碱式氯化镁沉淀。据文献介绍,碱式氯化镁存在多种组成结构,化学通式可表示为Mgx(OH)yClzmH2O(其中2x﹣y﹣z=0,0≤m≤6)。
(反思拓展)
(1)做镁与稀盐酸反应的实验时,为了不让试管中出现灰白色沉淀,镁条的用量_______。
(2)铁片和铜片放入稀硫酸中产生的现象也不相同,据此推测出铁的活动性比铜_____。