题目内容
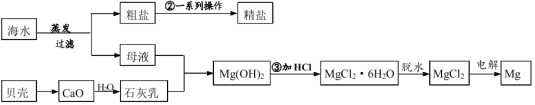
【题目】氯化锌是一种重要的工业原料,某化工厂用排放的废酸(主要成分为盐酸)和锌渣(主要含Zn、ZnO、FeSO4、CuSO4及部分不溶性杂质)生产氯化锌的工艺如下:

(1)请写出酸浸步骤发生的化学方程式_____(写一个)。
(2)在化学实验室中操作A和操作B都要必须用到的仪器是_____。
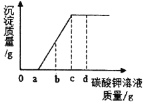
(3)“一次净化”中加入氯化钡可以将溶液中的_____(填离子符号)转化为滤渣除去;该过程加入氯酸钾时发生如下反应:(前面横线填化学计量数;后面横线填化学式)KClO3 + 6FeSO4 + 6HCl == KCl + 2Fe2(SO4)3 + 2 FeCl3 +_____、_____
【答案】![]() 或
或![]() 玻璃棒 SO42- 3 H2O
玻璃棒 SO42- 3 H2O
【解析】
(1)向锌渣中加入废酸,锌能与盐酸反应生成氯化锌和氢气,该反应的化学方程式为:![]() ;
;
氧化锌能与稀盐酸反应生成氯化锌和水,该反应的化学方程式为:![]() ;
;
(2)操作A实现了固液分离,故操作A为过滤,通过操作B,氯化锌溶液变为氯化锌晶体,故操作B为蒸发,过滤操作必须用到的仪器有:烧杯、漏斗、玻璃棒;蒸发必须用到的仪器有:玻璃棒、蒸发皿、酒精灯,故操作A和操作B都必须用到的仪器是:玻璃棒;
(3) 氯化钡能与硫酸根离子结合生成硫酸钡沉淀,故“一次净化”中加入氯化钡可以将溶液中的SO42-转化为滤渣除去,故填:SO42-;
(4)根据质量守恒定律,化学反应前后,原子的种类和数目不变,故将该化学方程式补全为:![]() ,故填:3、H2O;
,故填:3、H2O;

练习册系列答案
相关题目