题目内容
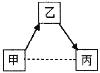
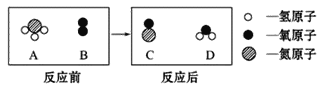
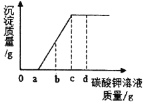
【题目】现有HCl和BaCl2的混合溶液,向其中逐滴滴入K2CO3溶液,生成沉淀质量与滴入K2CO3溶液质量的变化关系如右图所示。下列说法正确的是( )
A. 0~a段,溶液中发生的反应为BaCl2+K2CO3=2KCl+BaCO3↓
B. bg时,溶液中含H+、K+、Cl-三种离子
C. cg时,溶液中溶质只有KCl
D. dg时,溶液呈中性
【答案】C
【解析】
向盐酸和BaCl2的混合溶液中逐滴滴入K2CO3溶液时,K2CO3先和稀盐酸反应生成氯化钾、水和二氧化碳,后和BaCl2反应生成碳酸钡沉淀和氯化钾。
A、0~a段,K2CO3和稀盐酸反应,溶液中反应的化学方程式为:K2CO3+2HCl═2KCl +H2O+CO2↑,该选项说法不正确,故选项错误;
B、滴至b克时,已经发生了K2CO3溶液与氯化钡溶液反应生成碳酸钡沉淀和氯化钾,氯化钡有剩余,则溶液为氯化钡和氯化钾的混合溶液,溶液中含Ba2+、K+、C1-三种离子,故选项说法错误;
C、滴至c克时,K2CO3溶液与氯化钡溶液恰好完全反应,溶液呈中性,溶液中溶质只有氯化钾,故选项说法正确;
D、滴至d克时,K2CO3溶液过量,溶液中溶质是碳酸钾、氯化钠,溶液显碱性,故选项说法错误。
故选C。

【题目】如表是KCl和KNO3在不同温度下的溶解度.
温度/℃ | 20 | 30 | 40 | 50 | |
溶解度(g/100g水) | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | |
(1)硝酸钾的溶解度随温度的升高而_____(填“增大”或“减小”).
(2)用同一种方法可以使KCl、KNO3二种物质的溶液都析出晶体,该方法是_____.
(3)KCl、KNO3两种物质溶解度相等的温度在_____之间(用编号表示).
A 20℃以下 B 20℃~30℃ C 30℃~40℃ D 40℃~50℃
(4)20℃时,100g水中最多可溶解KCl的质量为_____;40℃时,将70gKCl的饱和溶液稀释成质量分数为20%的溶液,需加水_____g.
(5)将某温度下热的硝酸钾饱和溶液逐渐冷却至室温,下列有关量随时间变化趋势的图象不正确的是_____(用编号表示).