题目内容
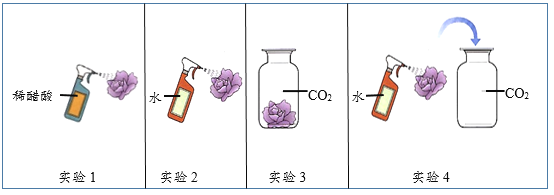
【题目】甲醇( CH3OH )是一种有毒,有酒的气味的可燃性液体。甲醇在氧气中不完全燃烧可发生如下反应: 8CH3OH+nO2![]() mCO2+2CO + 16H2O。若反应生成3.6g 水,请计算:
mCO2+2CO + 16H2O。若反应生成3.6g 水,请计算:
①m值是____;
②参加反应的氧气质量是________克?(写出规范计算步骤)
【答案】 6 4.4g
【解析】(1)根据质量守恒定律,在化学反应前后原子的种类和数目都没有改变。由已知反应物中C原子总数为8,生成物中C原子总数也应该为为8,则可以求得m=8-2=6;(2)
(2)设参加反应的氧气质量为X
8CH3OH+11O2![]() 6CO2+2CO+16H2O
6CO2+2CO+16H2O
11×32 16×18
![]() 3.6g
3.6g
![]()
![]() =4.4g
=4.4g
答:(1)m值是6;(2)参加反应的氧气质量是4.4g。

 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案【题目】过氧化氢在生产生活中有广泛应用。实验小组对过氧化氢的某些性质进行研究。
I.不稳定性
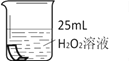
(1)如下图所示进行实验,过氧化氢分解的化学方程式为_______________,产生3.2g O2时分解的过氧化氢的质量为______ g。
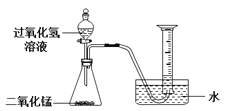
(2)能用排水法收集O2的原因是______。
(3)探究温度对过氧化氢分解速率的影响
同学们进行了如下的实验,实验数据如下表:
实验序号 | ① | ② | ③ |
H2O2溶液的浓度% | 30 | 30 | 30 |
H2O2溶液的体积/mL | 6 | 6 | 6 |
温度/℃ | 20 | 35 | 55 |
MnO2的用量/g | 0 | 0 | 0 |
收集O2的体积/mL | 0 | 1.9 | 7.8 |
反应时间 | 40min | 40min | 40 min |
由此得出的结论是_____________________________。
Ⅱ.腐蚀性
【查阅资料】H2O2溶液有腐蚀性。
【进行实验】
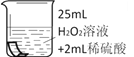
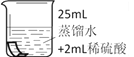
将铜片分别浸泡在3种溶液中进行实验,如下表。
编号 | ① | ② | ③ |
实验 |
|
|
|
一段时间后的现象 | 无明显变化 | 溶液变蓝,缓慢产生细小气泡 | 无明显变化 |
【解释与结论】
(4)实验①的作用是_____________________。
(5)铜片被腐蚀的反应如下,补全该反应的化学方程式。
Cu + H2O2+ H2SO4=== CuSO4 +_______。
【反思交流】
(6)某同学提出,实验②中,除发生(5)的反应外,还发生了一个反应导致有细小气泡产生,该反应的反应物为_______。
【题目】人类社会的发展离不开化学。请用学过的化学知识回答问题:
⑴.现有①液氧;②一氧化碳;③熟石灰;④石墨;⑤甲烷;⑥生石灰,从中选择适当的物质按照下列要求填空(填序号)可作干电池电极的是____;可用作食品干燥剂的是_____;常用来冶炼金属的是________;可用作火箭助燃剂的是________。
⑵.生活中用活性炭能除去冰箱内的异味,这是利用活性炭的_______性;饮用碳酸饮料时,打开瓶盖,发现有大量气泡溢出,从物理变化的角度解释为___________________。
⑶.下表是几种气体燃料的价格和热值:
燃烧物 | 煤气(主要成分是: CO) | 液化石油气 | 天然气 |
价格 | 1.4元/千克 | 6.0元/千克 | 1.8元/千克 |
热值 | 1.56×104kJ/kg | 4.5×104kJ/kg | 3.9×104kJ/kg |
若家庭使用,综合考虑,你将选用哪种燃料?_____理由是______、__________。丙烷也是一种很好的燃料,其化学式为C3H8。丙烷分子中C、H原子的个数比为_____,丙烷的摩尔质量为___,88g丙烷分子物质的量为_______。