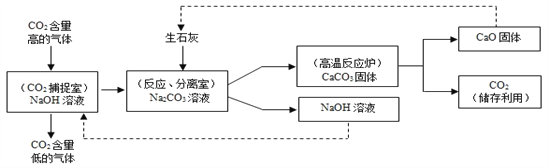
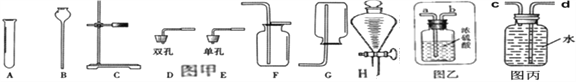
题目内容
【题目】如图中A、B、C、D、E、F分别表示六种物质,B、C、D、F分别属于酸、碱、盐、氧化物四种类别中的一种,A是目前世界上年产量最高的金属,B是可溶性银盐,D与E发生的反应属于中和反应。(图中用“”或“”表示两种物质之间能发生化学反应,用“→”或“”表示一种物质可以转化为另一种物质,部分反应物、生成物及反应条件已略去,图中部分反应需在溶液中进行)。请写出:

(1)B物质的化学式(或溶质的化学式):__________;
(2)E→F的化学反应方程式:______________________________________。
【答案】 AgNO3 H2SO4 + 2NaOH = Na2SO4 + 2H2O
【解析】本题主要考查物质的鉴别、推断;书写化学方程式。可以依据物质的性质进行根据物质间相互反应,确定反应的个数,然后进行推断即可.
A是目前世界上年产量最高的金属,所以A的铁,B是可溶性银盐所以B是硝酸银,D与E发生的反应属于中和反应,A会与E反应,所以E可以是硫酸,E会转化为F,F会转化为D,D是碱,所以D是氢氧化钠,F是水,盐酸转化成的C会与硝酸银、铁反应,所以C是硫酸铜,经过验证。推导正确。所以B的化学式为:
AgNO3,E→F的化学反应方程式:H2SO4 + 2NaOH = Na2SO4 + 2H2O

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案【题目】硫酸铜溶液对过氧化氢的分解有催化作用,取一定质量8.5%的过氧化氢溶液倒入烧杯中,加入一定质量15%的硫酸铜溶液,过氧化氢完全分解,有关实验数据如表所示(不考虑气体在水中的溶解).请计算:
反应前 | 反应后 | ||
实验数据 | 烧杯和过氧化氢溶液的质量/g | 硫酸铜溶液的质量/g | 烧杯和烧杯中溶液的质量/g |
60 | 3.3 | 62.5 | |
(1)生成氧气的质量为________.
(2)反应后烧杯中溶液溶质的质量分数.(写出计算过程,结果精确到0.1%).