题目内容
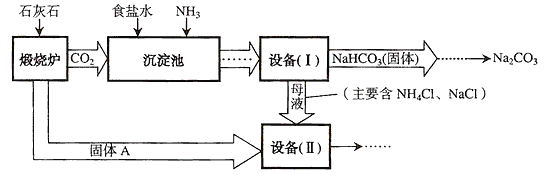
【题目】某废液中只含有Fe(NO3)2、Cu(NO3)2、Ba(NO3)2三种溶质。为了回收金属、保护环境,小科设计了如图方案(所加试剂均过量)。

A.固体a是铜
B.X 一定是Na2SO4
C.溶液B中含有的盐有Ba(NO3)2、NaNO3
D.若回收到6.4g固体a,则加入的铁屑质量为5.6g
【答案】C
【解析】A、根据金属活动性顺序的应用:位于前面的金属能把位于后面的金属从化合物的溶液中置换出来,故将铁加入到Fe(NO3)2、Cu(NO3)2、Ba(NO3)2的混合溶液中,铁能与硝酸铜反应生成铜和硝酸亚铁,即固体a是铜和过量的铁,错误;B、溶液A中含有硝酸亚铁和硝酸钡,氢氧化钠能与硝酸亚铁反应生成氢氧化亚铁沉淀和硝酸钠,故过滤后得到的沉淀b是氢氧化亚铁沉淀,溶液B中含有硝酸钠、氢氧化钠和硝酸钡。要将硝酸钡转化为沉淀,可加入含有硫酸根离子的物质,如:硫酸钠、硫酸钾等,错误;C、盐是由金属离子和酸根离子构成的,溶液B中含有硝酸钠、氢氧化钠和硝酸钡,硝酸钠和硝酸钡属于盐,氢氧化钠属于碱,正确;D、反应中加入的铁粉是过量的,由于固体a中除了含有铜以外,还含有铁,故若回收到6.4g固体a,则加入的铁屑质量一定大于5.6g,错误。故选C。

 名校课堂系列答案
名校课堂系列答案【题目】小柯探究pH对唾液淀粉酶活性的影响,其实验过程及结果如下:
组别 | A | B | C |
试管中依次 加入物质 | 1ml唾液 | 1ml唾液 | 1ml唾液 |
1ml盐酸溶液 | 1ml蒸馏水 | 1ml氢氧化钠溶液 | |
2ml淀粉溶液 | 2ml淀粉溶液 | 2ml淀粉溶液 | |
水浴10分钟 | 37℃ | 37℃ | 37℃ |
各滴入2滴 碘液后的现象 | 变蓝 | 不变蓝 | 不变蓝 |
(1)B组实验不变蓝的原因是____________________。小柯观察到C组也不变蓝,认为氢氧化钠对酶的活性没有影响。老师提示他:“氢氧化钠会影响酶的活性。”那么,是什么原因导致C组没变蓝?小柯进一步分析并做出猜想。
猜想一:氢氧化钠变质。
猜想二:氢氧化钠与碘发生了化学反应。
……
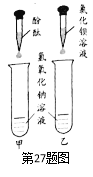
(2)小柯按图甲实验,看到溶液变红,认为氢氧化钠没有变质。小常认为他的结论是
错误的,理由是_________________________。
在小常的建议下,小柯按乙实验,溶液中没有沉淀产生,从而排除了猜想一。
(3)在原来C组实验基础上,只要继续_______________________(写出操作和现象),就可以证明猜想二正确。