题目内容
利用工业煤制乙二醇(重要的化工原料),因具有低成本、低能耗、低排放等特点而具有非常广阔的前景,该制备过程如下图所示。回答下列问题:
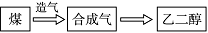
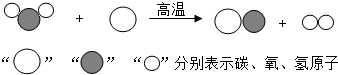
(1)“造气”过程的微观示意图如下,则制备合成气的化学方程式为________________。

(2)合成气有还原性,可用于冶炼钢铁。请写出合成气与Fe2O3反应的一个化学方程式:________________________________________________________________________。
(3)合成气在 不同催化剂作用下,可以合成不同的物质。仅用合成气为原料不可能得到的物质是______(填字母序号)。
不同催化剂作用下,可以合成不同的物质。仅用合成气为原料不可能得到的物质是______(填字母序号)。
A.草酸(HOOCCOOH)
B .甲醇(CH2OH)
.甲醇(CH2OH)
C.尿素[CO(NH2)2]
(4)从煤直接作燃料到用煤制取乙二醇,你得到的启示是__________________________。
解析:(1)属于图示类信息、处理本题的关键是能将图示中的结构改写为化学式,反应物“ ”、“
”、“ ”,即H2O、C,生成物“
”,即H2O、C,生成物“ ”、“
”、“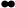 ”,即CO、H2;
”,即CO、H2;
(2)CO与Fe2O3高温生成铁和二氧化碳,H2与Fe2O3在高温下生成铁和H2O;
(3)根据反应前后元素种类不变,不可能得到含氮元素的尿素;
(4)化学对资源的开发利用、促进社会发展起着重要作用。
答案:(1)C+H2O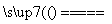 CO+H2 (2)Fe2O3+3H2
CO+H2 (2)Fe2O3+3H2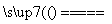 2Fe+3H2O或Fe2O3+3CO
2Fe+3H2O或Fe2O3+3CO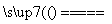 2Fe+3CO2 (3)C (4)化学能指导人类合理利用资源(其他合理答案也可)
2Fe+3CO2 (3)C (4)化学能指导人类合理利用资源(其他合理答案也可)

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 利用工业煤制乙二醇(重要的化工原料),因具有低成本、低能耗、低排放等特点而具有非常广阔的前景,该制备过程如右图所示.回答下列问题:
利用工业煤制乙二醇(重要的化工原料),因具有低成本、低能耗、低排放等特点而具有非常广阔的前景,该制备过程如右图所示.回答下列问题: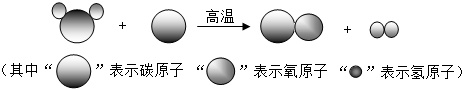


 利用工业煤制乙二醇(重要的化工原料),因具有低成本、低能耗、低排放等特点而具有非常广阔的前景,该制备过程如图所示.回答下列问题:
利用工业煤制乙二醇(重要的化工原料),因具有低成本、低能耗、低排放等特点而具有非常广阔的前景,该制备过程如图所示.回答下列问题: