题目内容
【题目】产品(CuCl)广泛应用于化学工业生产。CuC1是一种白色固体,难溶于乙醇和水,可溶于氯离子浓度较大的溶液,在潮湿空气中易氧化变质。以硫化铜精矿为原料生产CuC1的工艺过程如下图所示:
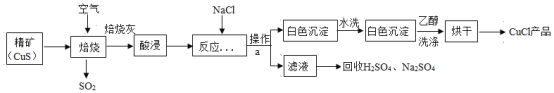
信息提示:(1).酸浸时发生的反应:CuO+H2SO4== CuSO4+H2O;(2).乙醇与水任意比互溶;(3).乙醇与CuC1不发生化学反应。
(1)产品CuCl中铜的化合价是____________。
(2)焙烧前对精矿进行粉碎,其目的是_________。
(3)CuS精矿经250℃低温培烧后生成CuO,该步骤中反应的化学方程式是________。
(4)操作a的名称是_________;进行该操作时玻璃棒的作用是________;本流程中可以循坏利用的物质(水除外)是___________(写化学式)。
(5)用“水洗”的目的是_____________,“乙醇洗涤”的目的是____________。
【答案】+1 增大精矿与空气的接触面积 2CuS+3O2![]() 2CuO+2SO2 过滤 引流 H2SO4 除去附在沉淀表面的硫酸钠、硫酸杂质 除去附在沉淀表面的水及防止在潮湿空气中氧化变质
2CuO+2SO2 过滤 引流 H2SO4 除去附在沉淀表面的硫酸钠、硫酸杂质 除去附在沉淀表面的水及防止在潮湿空气中氧化变质
【解析】
(1)在CuCl中铜的化合价为正价,那么氯元素的化合价为-1价。设CuCl中铜的化合价为X。则X-1=0,解得X=+1。
(2)焙烧前对精矿进行粉碎,其目的是增大精矿与空气的接触面积。
(3)CuS精矿经250℃低温培烧后生成CuO,该步骤中反应的化学方程式是2CuS+3O2![]() 2CuO+2SO2 。
2CuO+2SO2 。
(4)通过操作a后得到白色沉淀和滤液,固液分离,所以操作a的名称是过滤;在过滤操作中玻璃棒的作用是引流;在滤液中可以回收H2SO4,在酸浸中用到H2SO4,所以本流程中可以循坏利用的物质(水除外)是H2SO4。
(5)因为白色固体表面残留有硫酸钠、硫酸杂质,用“水洗”的目的是除去附在沉淀表面的硫酸钠、硫酸杂质;CuC1难溶于乙醇且在潮湿空气中易氧化变质,因此,“乙醇洗涤”的目的是除去附在沉淀表面的水及防止在潮湿空气中氧化变质。

 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案