题目内容
【题目】宏观和微观相结合是认识物质结构的有效方法之一。
(1)1~18号元素原子最外层电子数与原子序数的关系如下图。X、Y、Z、W表示的元素分别为O、Mg、Al、Cl,试回答下列问题:
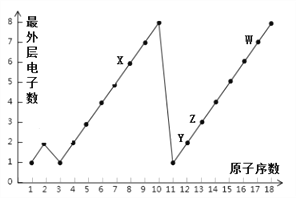
①单质W2与单质Y的反应中,Y原子______ (填“得到“成“失去”)电子,其形成的离子符号为_____________。
②X、Z形成的化合物为______(填物质名称)。
③原子序数分别为2和10的原子最外层电子数不一样,但在元素周期表中都处于同一族,从原子结构上分析其原因:____________
(2)下图为Zn和 NaHSO4溶液反应的微观示意图,回答下列问题:
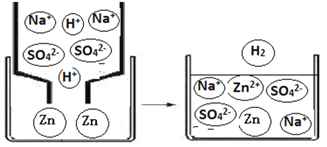
①实际与Zn反应的粒子是____________
②写出烧杯中发生反应的化学方程式:_________________
【答案】 失去 Mg2+ 三氧化二铝(或填氧化铝) 最外层都是相对稳定结构(或最外层电子数都填满) H+ Zn +2NaHSO4 = ZnSO4 + Na2SO4 + H2↑
【解析】本题考查了原子核外电子排布,化学反应的微观模拟示意图。解题的关键是依据原子核外电子排布的规律、化学反应的实质并结合图示依据相关的知识进行分析。
(1)①Y是镁元素,根据1~18号元素原子最外层电子数与原子序数的关系图,可知Y原子的最外层电子数为2,在化学变化中易失去2个电子,形成稳定结构,离子符号为:Mg2+;
②铝元素和氧元素形成的化合物中,铝元素化合价是+3,氧元素化合价是-2,形成的化合物的化学式是Al2O3,物质的名称是三氧化二铝(或填氧化铝);
③原子序数分别为2和10的原子最外层电子数不一样,但在元素周期表中都处于同一族的原因是最外层都是相对稳定结构(或最外层电子数都填满);
(2)①由图中信息可知,发生改变的氢离子和锌原子,其他微粒没有改变,实际与Zn反应的粒子是H+;
②由图中信息可知,烧杯中发生反应的是Zn和 NaHSO4反应生成ZnSO4 、Na2SO4 和 H2,化学方程式是Zn +2NaHSO4 = ZnSO4 + Na2SO4 + H2↑。