题目内容
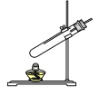
【题目】某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功。
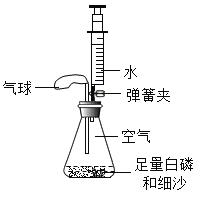
[查阅资料]当温度达到40℃以上并与氧气接触时,白磷即可以燃烧起来且产物与红磷燃烧后相同。
[提出问题]氧气体积约占空气总体积的多少?
[实验准备]锥形瓶内空气体积为200mL,注射器中水的体积为50mL,该装置气密性良好。
[实验探究]装入药品,按图所示连接好仪器,夹紧弹簧夹.先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出。
[现象分析]
(1)足量的白磷在锥形瓶中未能全部燃烧,说明瓶内剩余气体_____燃烧(填“支持”或“不支持”)。写出白磷燃烧的文字(或符号)表达式:_____。
(2)在整个实验过程中,可观察到气球的变化是:_____。
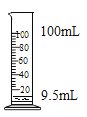
(3)待白磷熄灭、锥形瓶冷却到室温后,打开弹簧夹,还可观察到的现象是:①注射器中的水自动喷射出来,②当注射器中的水还剩约10mL时停止下流。导致这些现象发生的原因是:_____;_____。
[得出结论]氧气约占空气总体积的五分之一。
【答案】不支持 磷+氧气![]() 五氧化二磷 气球先膨胀后缩小并变瘪 白磷燃烧消耗氧气,瓶内气体减少压强变小 瓶内氧气约占40mL
五氧化二磷 气球先膨胀后缩小并变瘪 白磷燃烧消耗氧气,瓶内气体减少压强变小 瓶内氧气约占40mL
【解析】
(1)足量的白磷在锥形瓶中未能全部燃烧,说明瓶内剩余气体不支持燃烧。白磷燃烧生成五氧化二磷,反应的文字表达式为:磷+氧气![]() 五氧化二磷。
五氧化二磷。
(2)红磷燃烧放出大量的热,开始装置内压强变大,气球膨胀;红磷燃烧消耗氧气,无气体生成,温度逐渐冷却过程中,压强逐渐变小,气球也逐渐变小,由于冷却至室温时,压强小于开始的压强,所以气球和原来相比变瘪,故在整个实验过程中,可观察到气球的变化是:气球先膨胀后缩小并变瘪。
(3)待白磷熄灭、锥形瓶冷却到室温后,锥形瓶内压强变小,打开弹簧夹,水进入锥形瓶,由于消耗多少体积的氧气,进入多少体积的水,锥形瓶中氧气的体积为:200mL×![]() =40mL,故注射器中的水自动喷射出来,当注射器中的水还剩约50mL-40mL=10mL时停止下流。
=40mL,故注射器中的水自动喷射出来,当注射器中的水还剩约50mL-40mL=10mL时停止下流。
[得出结论]氧气约占空气总体积的五分之一。

【题目】研究和控制化学反应条件有重要意义。
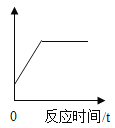
(1)同学们想探究过氧化氢的浓度对反应速率的影响。在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间。
实验 | 30%双氧水 的质量(g) | 加入的水 的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
1 | 10 | 20 | 5 | 200 |
2 | 20 | 20 | 5 | 100 |
3 | 30 | 20 | ______________ | 67 |
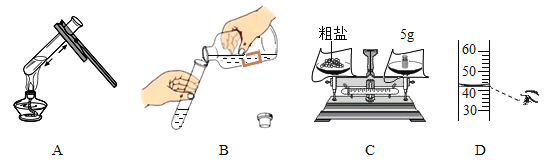
①取用二氧化锰的仪器是 ______。
②二氧化锰在过氧化氢的分解中起_________作用。
③实验3中,加入的二氧化锰质量为_________g。
④相同条件下,实验3产生氧气的速率最快,说明_________。
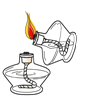
(2)同学通过查阅资料得知,过氧化氢在70℃以上会较快分解产生氧气。为了验证加热过氧化氢也可以产生氧气,同学们选择右图装置(气密性良好)进行实验。实验中观察试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是___________,同学分析原因后,采用了______法收集气体,再检验,证明加热双氧水也可产生氧气。