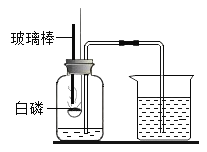
题目内容
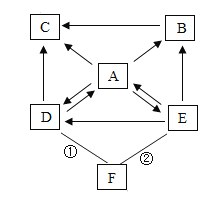
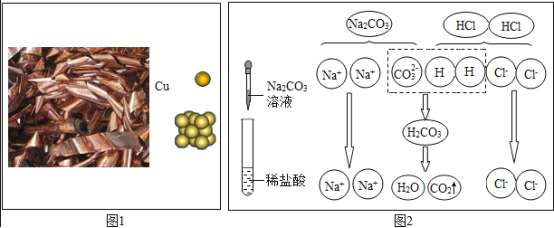
【题目】经过“碱的化学性质”的学习,小明同学用如图所示的示意图归纳总结了NaOH四条化学性质。
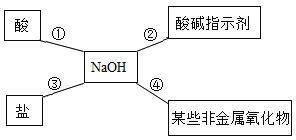
(1)反应①属于的基本反应类型是____________。
(2)为了验证反应②,小明同学向NaOH溶液中滴入无色酚酞试液,观察到无色酚酞试液变为红色,使无色酚酞试液变为红色的微粒是______________(填微粒符号)。
(3)为了验证反应③能够发生,应选用的试剂是______________.
A KNO3
B NaCl
C CuSO4
D Na2CO3
(4) NaOH溶液露置于空气中易变质,所以必须密封保存,请你写出NaOH溶液变质的化学方程式:____________。
【答案】复分解反应 OH- C ![]()
【解析】
(1)反应①为酸与碱的反应,酸与碱作用生成盐和水的反应,叫做中和反应,中和反应属于复分解反应,故填:复分解反应;
(2)无色酚酞试液遇碱变蓝,碱在水溶液中都能电离出氢氧根离子,故能使紫色石蕊试液变蓝的粒子是:OH-;
(3)A、硝酸钾与氢氧化钠不反应,无法验证,不符合题意;
B、氯化钠与氢氧化钠不反应,无法验证,不符合题意;
C、硫酸铜能与氢氧化钠反应生成氢氧化铜和硫酸钠,硫酸铜是由金属离子和酸根离子组成的化合物,属于盐,故可以验证反应③能够发生,符合题意;
D、碳酸钠与氢氧化钠不反应,无法验证,不符合题意。
故选C;
(4)氢氧化钠容易与空气中的二氧化碳反应生成碳酸钠和水,该反应的化学方程式为:![]() 。
。

 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
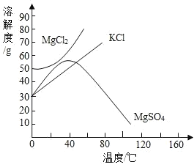
名校名师培优作业本加核心试卷系列答案【题目】依据下列![]() 时的实验和数据回答。已知
时的实验和数据回答。已知![]() 时,NaCl和NaNO3的溶解度分别为36g和88g。
时,NaCl和NaNO3的溶解度分别为36g和88g。
| 序号 |
|
|
|
|
|
固体种类 | NaCl | NaCl | NaNO3 | NaNO3 | NaNO3 | |
固体的质量 | 30 | 60 | 30 | 60 | 90 | |
水的质量 | 100 | 100 | 100 | 100 | 100 |
下列关于![]() 所得溶液的说法不正确的是
所得溶液的说法不正确的是![]()
![]()
A. 溶质质量:![]()
B. 溶液质量:![]()
C. 溶质质量分数:![]()
D. ![]() 中溶质与溶剂的质量比为9:10
中溶质与溶剂的质量比为9:10