题目内容
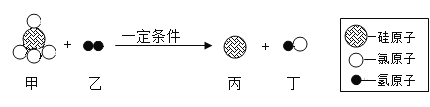
【题目】下图化学反应的溶液颜色变化体现了“魔法世界,魅力化学”。请回答“

(1)溶液X是______(填“酸”、“碱”或“盐”),试剂A的名称是____________。
(2)若X是稀硫酸,B是氧化物,则B的化学式为________________________。
(3)若X是稀盐酸,C是单质,则C的名称为___________________。
(4)若X是稀硫酸,D是碱,则X与D反应的化学方程式为____________________。
【答案】酸 石蕊试液 Fe2O3 铁 H2SO4+Cu(OH)2═CuSO4+2H2O
【解析】
分析可知黄色溶液、蓝色溶液、浅绿色溶液都是盐的溶液,能够三种物质反应生成可溶性的且带颜色的盐的只有酸的溶液,
(1)X应该为酸,和酸反应生成红色溶液的就是紫色石蕊试液;
(2)若X为稀硫酸,B为氧化物,它们生成的是黄色溶液,我们知道的黄色溶液应该为铁盐的溶液,所以B应该为氧化铁;
(3)我们所学的浅绿色的溶液只有亚铁盐的溶液,当X为稀盐酸,C为单质时,那么可以知道C应该为单质铁;
(4)我们所学的蓝色溶液只有铜盐的溶液,所以在这里和稀硫酸反应的碱应该为氢氧化铜,故本题答案为:H2SO4+Cu(OH)2═CuSO4+2H2O。

 小学能力测试卷系列答案
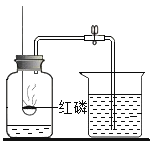
小学能力测试卷系列答案【题目】请根据下列实验图回答问题
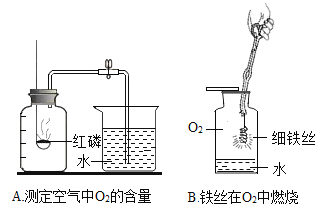
(1)上述两个实验中,水主要对实验仪器起到安全保护作用的是_______(填序号)。
(2)①请写出A实验中发生反应的化学方程式______________________________;
②请写出B实验中的实验现象______________________________;
(3)A实验中,若进入集气瓶中的水小于其体积的五分之一,原因____________________
(4)学校某学习小组的同学对影响过氧化氢分解快慢的因素进行探究。
分别取5 mL H2O2溶液进行实验,测定产生4 mL O2所需时间,实验结果记录如下:
实验 序号 | H2O2溶液的浓度 | 温度 /℃ | MnO2粉 末用量/g | 反应 时间 |
① | 30% | 35 | 0 | t1 |
② | 30% | 55 | 0 | t2 |
③ | 5% | 20 | m | 3 s |
④ | 15% | 20 | 0.1 | 1 s |
I.对比①②可知:其它条件相同时,温度越高,过氧化氢分解越快,则t1________t2(填“>”、“=”或“<”)。
II.若要探究过氧化氢分解快慢与过氧化氢溶液浓度有关,则m的值为______,选择的实验序号为__________,合理的结论是________________________________。