题目内容
【题目】请根据下列实验图回答问题
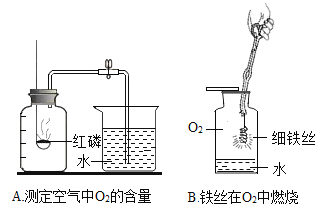
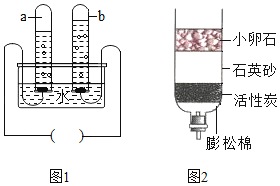
(1)上述两个实验中,水主要对实验仪器起到安全保护作用的是_______(填序号)。
(2)①请写出A实验中发生反应的化学方程式______________________________;
②请写出B实验中的实验现象______________________________;
(3)A实验中,若进入集气瓶中的水小于其体积的五分之一,原因____________________
(4)学校某学习小组的同学对影响过氧化氢分解快慢的因素进行探究。
分别取5 mL H2O2溶液进行实验,测定产生4 mL O2所需时间,实验结果记录如下:
实验 序号 | H2O2溶液的浓度 | 温度 /℃ | MnO2粉 末用量/g | 反应 时间 |
① | 30% | 35 | 0 | t1 |
② | 30% | 55 | 0 | t2 |
③ | 5% | 20 | m | 3 s |
④ | 15% | 20 | 0.1 | 1 s |
I.对比①②可知:其它条件相同时,温度越高,过氧化氢分解越快,则t1________t2(填“>”、“=”或“<”)。
II.若要探究过氧化氢分解快慢与过氧化氢溶液浓度有关,则m的值为______,选择的实验序号为__________,合理的结论是________________________________。
【答案】)B 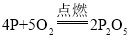 剧烈燃烧,火星四射 ,生成黑色固体 红磷量不足或装置气密性不好或没有冷却到室温就打开弹簧夹(合理即可) > 0.1 ③④ 其它条件相同时,过氧化氢溶液浓度越高,分解越快(表述合理即可)
剧烈燃烧,火星四射 ,生成黑色固体 红磷量不足或装置气密性不好或没有冷却到室温就打开弹簧夹(合理即可) > 0.1 ③④ 其它条件相同时,过氧化氢溶液浓度越高,分解越快(表述合理即可)
【解析】
(1)A实验中,水的作用是用水的体积来验证氧气的体积;B实验中,水的作用是防止高温溅落物炸裂瓶底;
(2)①红磷燃烧生成五氧化二磷,反应的化学方程式: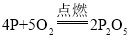 ;
;
②实验B中铁丝在氧气中燃烧的现象是剧烈燃烧、火星四射,生成黑色固体,放出大量的热;
(3)红磷的量必须充足的目的是尽可能完全消耗装置内的氧气,使结果更准确,实验中发现打开弹簧夹进入集气瓶中水的体积小于其体积的五分之一,原因可能是:红磷量不足或装置气密性不好或没有冷却到室温就打开弹簧夹;
(4)I.对比①②可知,其他条件均相同,②实验温度较高,过氧化氢分解较快,因此t2所需时间较短;
II.分析表中数据可知,m是0.1g;③④两组实验唯一的不同是过氧化氢溶液溶质质量分数不同,因此能得出过氧化氢分解快慢与溶质质量分数有关;能得出的合理结论是:其他条件相同时,H2O2溶液的溶质质量分数越高,过氧化氢分解越快。

 名校课堂系列答案
名校课堂系列答案