题目内容
【题目】科学家在-100℃合成了物质X(分子模型如图,其中 ![]() 代表碳原子,
代表碳原子,![]() 代表氢原子)。
代表氢原子)。
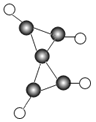
(1)物质 X 的化学式为_______。(提示:碳元素写在前面)
(2)1个物质X_______构成。
(3)物质X中碳、氢元素的质量比为_______(最简整数比)。
(4)物质X的相对分子质量为_______。
(5)该物质中氢元素的质量分数为_______。(计算结果精确到 0.1%)
【答案】C5H4 分子是由5个碳原子和4个氢原子 15:1 64 6.3%
【解析】
(1)由分子模型图,其中![]() 代表碳原子,
代表碳原子,![]() 代表氢原子,1个该化合物的分子是由5个碳原子和4个氢原子构成的,其化学式为:C5H4;
代表氢原子,1个该化合物的分子是由5个碳原子和4个氢原子构成的,其化学式为:C5H4;
(2)由题可知物质X是由分子构成的,而一个物质X分子是由5个碳原子和4个氢原子构成;
(3)物质X中碳、氢元素的质量比为(12×5):(1×4)=15:1;
(4)物质X的相对分子质量为:12×5+1×4=64;
(5)该物质中氢元素的质量分数=![]() 。
。

练习册系列答案
 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目