题目内容
在20℃时,向100g KNO3饱和溶液中加入5g KNO3晶体,则( )
| A、KNO3晶体的质量减少 |
| B、溶液中KNO3的质量分数增大 |
| C、KNO3晶体的质量不变 |
| D、KNO3的溶解度变化 |
考点:饱和溶液和不饱和溶液,固体溶解度的概念
专题:溶液、浊液与溶解度
分析:饱和溶液是指在一定温度下、一定量的溶剂里,不能再继续溶解这种溶质的溶液;则在一瓶KNO3的饱和溶液中,当温度不变时,加入少量该溶质晶体,硝酸钾晶体不能继续溶解,据此进行分析判断.
解答:解:
A、向100g KNO3饱和溶液中加入5g KNO3晶体,当温度不变时,加入少量该溶质晶体,该晶体不能继续溶解,则晶体的质量不变,故选项错误.
B、向100g KNO3饱和溶液中加入5g KNO3晶体,当温度不变时,加入少量该溶质晶体,该晶体不能继续溶解,则晶体的质量不变,溶剂质量不变,溶液中KNO3的质量分数不变,故选项错误.
C、向100g KNO3饱和溶液中加入5g KNO3晶体,当温度不变时,加入少量该溶质晶体,该晶体不能继续溶解,则晶体的质量不变,故选项正确.
D、向100g KNO3饱和溶液中加入5g KNO3晶体,当温度不变时,则溶解度不变,故选项错误.
答案:C.
A、向100g KNO3饱和溶液中加入5g KNO3晶体,当温度不变时,加入少量该溶质晶体,该晶体不能继续溶解,则晶体的质量不变,故选项错误.
B、向100g KNO3饱和溶液中加入5g KNO3晶体,当温度不变时,加入少量该溶质晶体,该晶体不能继续溶解,则晶体的质量不变,溶剂质量不变,溶液中KNO3的质量分数不变,故选项错误.
C、向100g KNO3饱和溶液中加入5g KNO3晶体,当温度不变时,加入少量该溶质晶体,该晶体不能继续溶解,则晶体的质量不变,故选项正确.
D、向100g KNO3饱和溶液中加入5g KNO3晶体,当温度不变时,则溶解度不变,故选项错误.
答案:C.
点评:本题难度不大,掌握饱和溶液的概念、特征并能灵活运用是正确解答本题的关键.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
溶洞中形态各异的石笋和钟乳石在形成过程,发生了多个化学反应,其中一个反应的化学方程式为:X+CO2+H2O═Ca(HCO3)2.则X的化学式为( )
| A、CaCO3 |
| B、Ca(OH)2 |
| C、CaO |
| D、Ca |
茶多酚是形成茶叶色香味的主要成份之一,也是茶叶中有保健功能的主要成份之一.研究表明,茶多酚具有解毒和抗辐射作用,其化学式为C17H19N3O,下列有关说法不正确的是( )
| A、茶多酚由4种元素组成 |
| B、茶多酚中碳氢氮氧四种元素的原子个数比是17:19:3:1 |
| C、茶多酚由17个碳原子、19个氢原子、3个氮原子和1个氧原子构成 |
| D、茶多酚中碳元素的质量分数为72.6% |
逻辑推理是一种重要的化学思维方法,以下推理合理的是( )
| A、因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有C和H |
| B、因为H2O和H2O2的组成元素相同,所以它们的化学性质相同 |
| C、因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件 |
| D、因为碱溶液呈碱性,所以呈碱性的溶液一定都是碱溶液 |
(NH4)3PO4是常见的复合肥,磷酸铵中氮元素的化合价为( )
| A、-3 | B、0 | C、+3 | D、+5 |
某反应的微观示意图(一种小球代表一种元素的原子),下列说法错误的是( )
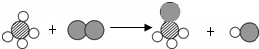

| A、该反应符合质量守恒定律 |
| B、该反应的本质是原子的重新组合 |
| C、该反应中的反应物都是化合物 |
| D、该反应前后分子的种类发生改变 |