题目内容
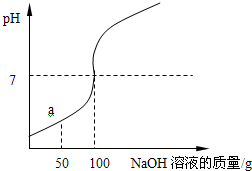 为测定某稀盐酸溶液溶质的质量分数,取100g该溶液于烧杯中,向烧杯中滴入16%的NaOH溶液,用pH计测得滴入NaOH溶液质量与pH的关系如图所示.
为测定某稀盐酸溶液溶质的质量分数,取100g该溶液于烧杯中,向烧杯中滴入16%的NaOH溶液,用pH计测得滴入NaOH溶液质量与pH的关系如图所示.(1)在a点时,烧杯中溶液的溶质是
(2)通过计算求盐酸溶液溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)由图示可知,滴加氢氧化钠溶液到100克时,氢氧化钠溶液与稀盐酸完全反应,当滴加稀盐酸至图中a点时,稀盐酸还没有完全反应,这时溶液中的溶质就有氯化钠和氯化氢两种.
(2)根据反应的氢氧化钠的质量,利用化学方程式求出反应的盐酸的溶质的质量.进而求出盐酸的质量分数.
(2)根据反应的氢氧化钠的质量,利用化学方程式求出反应的盐酸的溶质的质量.进而求出盐酸的质量分数.
解答:解:(1)由图示可知,滴加氢氧化钠溶液到100克时,氢氧化钠溶液与稀盐酸完全反应,当滴加稀盐酸至图中a点时,稀盐酸还没有完全反应,盐酸就有剩余,这时溶液中的溶质就有氯化钠和氯化氢两种.
故答案为:NaCl和HCl;
(2)设100g稀盐酸中含HCl的质量为x
NaOH+HCl═NaCl+H2O
40 36.5
100g×16% x
=
x=14.6g
所用稀盐酸的溶质质量分数=
×100%=14.6%
答:所用稀盐酸的溶质质量分数为14.6%.
故答案为:NaCl和HCl;
(2)设100g稀盐酸中含HCl的质量为x
NaOH+HCl═NaCl+H2O
40 36.5
100g×16% x
| 40 |
| 100g×16% |
| 36.5 |
| x |
x=14.6g
所用稀盐酸的溶质质量分数=
| 14.6g |
| 100g |
答:所用稀盐酸的溶质质量分数为14.6%.
点评:做这类题目要会看折点,折点是指图象在变化过程中方向发生了大的转变的那个点.它的出现往往是两个变量中某一变量单方面停止造成的.如果图象涉及化学反应,折点通常是该反应的结束点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
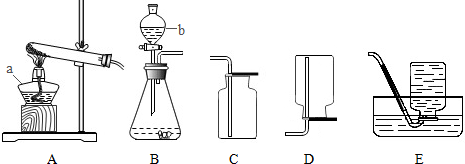
 走进化学实验室,你会抑制不住内心的喜悦,想马上开始做自己喜欢的实验.如图是八位同学在实验室中的一些行为,其中存在的安全隐患(至少写出四种):
走进化学实验室,你会抑制不住内心的喜悦,想马上开始做自己喜欢的实验.如图是八位同学在实验室中的一些行为,其中存在的安全隐患(至少写出四种):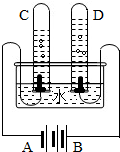 请根据题目要求回答下列问题.
请根据题目要求回答下列问题.