题目内容
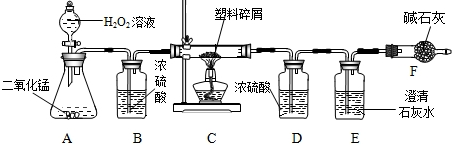
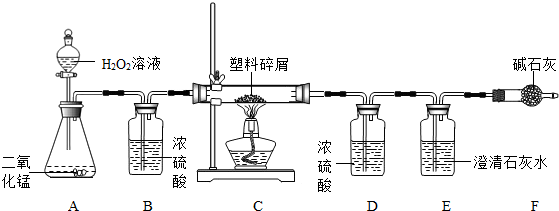
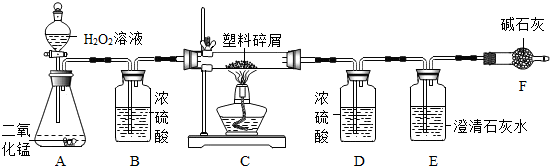
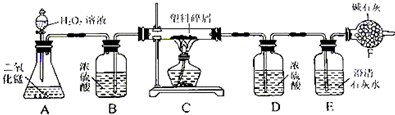
由于大量使用一次性塑料方便袋造成的“白色污染”,已成为一个严重的社会问题.某化学研究小组的同学欲对某种塑料袋的组成进行分析探究(资料显示该塑料只含C、H两种元素),他们设计了如下图所示的实验装置,使该塑料试样在纯氧中燃烧,观察实验现象,分析有关数据,推算元素含量.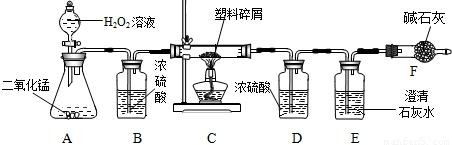
(1)仪器A中所发生的反应化学方程式为______ 2H2O+O2↑
【答案】分析:本题是利用双氧水的分解产生O2,再根据塑料燃烧产物来验证其组成的.
(1)双氧水在二氧化锰的催化作用下分解得到氧气
(2)仪器B 中装有浓硫酸,具有吸水性,可干燥氧气
(3)仪器E中有澄清石灰水,而二氧化碳能使澄清石灰水变浑浊
(4)可根据元素守恒,水是塑料的燃烧产物,水中的H元素和塑料中H元素质量相同
(5)若装置中没有连接仪器B,在A装置中的水会在D中和反应生成的水一起被吸收,使水质量增大
解答:解:(1)双氧水分解得到氧气和水,故答案为:2H2O2 2H2O+O2↑
2H2O+O2↑
(2)浓硫酸具有吸水性,故答案为:干燥氧气(或吸收水分)
(3)二氧化碳能使澄清石灰水变浑浊,故答案为:澄清石灰水变浑浊
(4)由元素守恒,塑料中H元素的质量为:a× ×100%=
×100%= ,故答案为:
,故答案为:
(5)没有干燥氧气,使水在D中吸收,质量增大,故答案为:偏大
点评:本实验题要利用元素守恒的思想,还要特别注意在验证生成物水时要排除从溶液中携带的水的干扰.
(1)双氧水在二氧化锰的催化作用下分解得到氧气
(2)仪器B 中装有浓硫酸,具有吸水性,可干燥氧气
(3)仪器E中有澄清石灰水,而二氧化碳能使澄清石灰水变浑浊
(4)可根据元素守恒,水是塑料的燃烧产物,水中的H元素和塑料中H元素质量相同
(5)若装置中没有连接仪器B,在A装置中的水会在D中和反应生成的水一起被吸收,使水质量增大
解答:解:(1)双氧水分解得到氧气和水,故答案为:2H2O2
 2H2O+O2↑
2H2O+O2↑(2)浓硫酸具有吸水性,故答案为:干燥氧气(或吸收水分)
(3)二氧化碳能使澄清石灰水变浑浊,故答案为:澄清石灰水变浑浊
(4)由元素守恒,塑料中H元素的质量为:a×
 ×100%=
×100%= ,故答案为:
,故答案为:
(5)没有干燥氧气,使水在D中吸收,质量增大,故答案为:偏大
点评:本实验题要利用元素守恒的思想,还要特别注意在验证生成物水时要排除从溶液中携带的水的干扰.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目