题目内容
【题目】某实验小组想通过实验证明某燃煤烟气中含有CO2,SO2
(查阅资料](1)二氧化硫能使紫红色的稀高锰酸钾溶液褪色,二氧化碳不能。
(2)二氧化硫能和可溶性碱溶液反应生成亚硫酸盐。
(3)CaSO3难溶于水;Na2SO3易溶于水,水溶液显碱性。
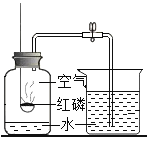
(实验验证]将燃煤烟气通过如图装置进行实验:
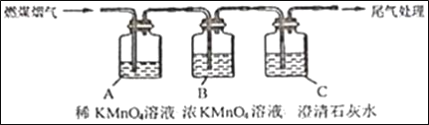
请回答下列问题:
(1)SO2能使高锰酸钾溶液褪色,反应方程式为:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2X,则X的化学式是_____;高锰酸钾中锰元素的化合价为_____。
(2)实验中观察到装置A溶液褪色,装置B溶液不褪色,装置C中出现_____,则烟气中含有SO2、CO2
(3)如图装置B中用了过量的浓高锰酸钾溶液不褪色,则说明_____;燃煤烟气中可能还含有_____气体,所以实验中最后要进行尾气处理。
(继续探究)工业上常用氢氧化钠或氢氧化钙等作为吸收剂,对燃煤烟气进行脱硫处理,实验小组想利用传感器再探究它们对燃煤烟气的吸收情况,实验步骤如下:
I.如图M所示装置的气密性良好,两瓶250mL的烧瓶内收满燃煤烟气,贴上标签瓶①瓶②,对应注射器内分别装有85mL的饱和石灰水、85mL的40%的氢氧化钠溶液;连接好装置和压强传感器。
Ⅱ.打开止水夹,两位同学同时迅速将注射器内85mL的液体注入各自烧瓶中,立即关闭止水夹。
Ⅲ.一段时间后,同时振荡烧瓶。观察到传感器定量实时地传回烧瓶内气压变化形成的图象情况如图N所示。
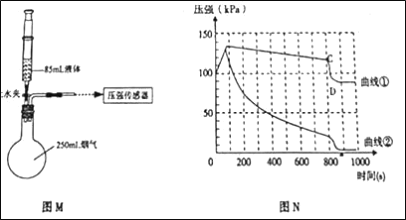
试回答下列问题:
(4)导致曲线①中CD段气压急速减小的操作是_____曲线②中反应的一个化学反应方程式为_____;曲线①和曲线②差异较大的原因_____,由此得出结论:吸收燃煤烟气较合适的是_____。(填字母编号:A.氢氧化钠溶液、B氢氧化钙溶液)。
(提出新问题)
实验后的废液处理问题:
若瓶②装置实验后,所得溶液中还含有氢氧化钠,则不能直接倒入下水道中。为探究瓶②装置实验后所得溶液中是否还含有氢氧化钠,同学们又进行了如下探究:
(5)将瓶②装置实验后所得溶液倒入烧杯中,加入足量的氯化钙溶液,目的是_____;过滤,向滤液中滴加酚酞试液,若观察到现象是_____,则还含有氢氧化钠,再处理至中性后再倒入下水道中。
【答案】H2S +7 石灰水变浑浊 二氧化硫已经除尽 一氧化碳 振荡烧瓶 2HaOH+CO2=Na2CO3+H2O(或2NaOH+SO2=Na2SO3+H2O) 氢氧化钙溶液中含有氢氧化钙的量很少,影响了二氧化碳、二氧化硫的吸收 A 除去Na2CO3、Na2SO3 溶液变红色
【解析】
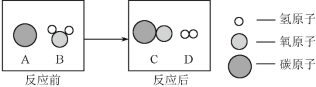
(1)在化学方程式:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2X中,反应物中:硫原子个数为5个,钾原子个数为2个,锰原子个数为2个,氢原子个数为4个,氧原子个数为20个;反应后生成物中:硫原子个数为3个,钾原子个数为2个,锰原子个数为2个,则X为:H2S;KMnO4中K为+1价,O为﹣2价,根据化合物中各元素化合价的代数和为0,则Mn为+7价;
(2)实验中观察到装置A溶液褪色,说明原混合气体中含有二氧化硫,装置B溶液不褪色,装置C中出现石灰水变浑浊,则烟气中含有SO2、CO2;
(3)如图装置B中用了过量的浓高锰酸钾溶液不褪色,则说明二氧化硫已经除尽,燃煤烟气还可能含有未完全燃烧的一氧化碳,防止进入空气污染环境,所以实验中最后要进行尾气处理;
(4)根据振荡烧瓶会加快二氧化碳的溶解,导致曲线①中CD段气压急速减小的操作是振荡烧瓶;二氧化硫、二氧化碳都可以和氢氧化钠反应反应的化学方程式为:2HaOH+CO2=Na2CO3+H2O,2NaOH+SO2=Na2SO3+H2O;氢氧化钙溶液中含有氢氧化钙的量很少,影响了二氧化碳、二氧化硫的吸收,所以曲线①和曲线②差异较大;由于氢氧化钠溶液吸收二氧化碳、二氧化硫比较多,所以吸收燃煤烟气用NaOH溶液较合适;
[提出新问题]
(5)因为Na2CO3、Na2SO3溶液呈碱性,要想验证溶液中是否含有氢氧化钠,要先除去Na2CO3、Na2SO3的干扰,可以通过加入足量的氯化钙溶液除去,过滤,向滤液中滴加酚酞试液,若观察到现象是溶液变红色,则还含有氢氧化钠。
故答案为:
(1)H2S+7;(2)石灰水变浑浊;(3)二氧化硫已经除尽一氧化碳;(4)振荡烧瓶 2HaOH+CO2=Na2CO3+H2O(或2NaOH+SO2=Na2SO3+H2O) 氢氧化钙溶液中含有氢氧化钙的量很少,影响了二氧化碳、二氧化硫的吸收 A;(5)除去Na2CO3、Na2SO3 溶液变红色

 互动课堂系列答案
互动课堂系列答案